题目内容
实验室需480mL 1.0mol/L的NaOH溶液,假如其他操作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是( )
| A、称取氢氧化钠20.0 g |
| B、定容时俯视观察刻度线 |
| C、移液时,对用于溶解氢氧化钠的烧杯没有进行冲洗 |
| D、移液用玻璃棒引流时,玻璃棒下端靠在容量瓶刻度线上方 |
考点:溶液的配制
专题:实验评价题
分析:配制一定物质的量浓度的溶液过程中,能引起误差的原因主要有:称量不准确、转移不完全、读数不符合要求、操作不规范等,可以根据错误操作对c=
的影响进行判断.
| n |
| V |
解答:
解:A.配制480mL溶液,需要选用500mL容量瓶,需要碳酸钠晶体的物质的量为1.0mol/L×0.5L=0.5mol,需要氢氧化钠的质量为:40g/mol×0.5mol=20g,称量氢氧化钠质量符合要求,不会产生误差,故A错误;
B.定容时俯视刻度线,导致配制的溶液的体积偏小,浓度偏高,故B正确;
C.没有洗涤烧杯,导致配制的溶液中溶质的物质的量减小,配制的溶液浓度偏低,故C错误;
D.玻璃棒下端靠在容量瓶刻度线上方,导致配制的溶液的体积偏大,浓度偏低,故D错误;
故选B.
B.定容时俯视刻度线,导致配制的溶液的体积偏小,浓度偏高,故B正确;
C.没有洗涤烧杯,导致配制的溶液中溶质的物质的量减小,配制的溶液浓度偏低,故C错误;
D.玻璃棒下端靠在容量瓶刻度线上方,导致配制的溶液的体积偏大,浓度偏低,故D错误;
故选B.
点评:本题考查了配制一定浓度的溶液的误差分析,主要是熟练掌握常见误差的分析方法,本题难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在无色强酸性溶液中,下列各组离子一定能大量共存的是( )
| A、Na+、K+、Cl-、SO42? |
| B、Cu2+、K+、SO42-、NO3- |
| C、K+、NH4+、SO42-、CO32? |
| D、Ba2+、Na+、Cl-、SO42- |
下列事实与胶体性质无关的是( )
| A、在豆浆里加入盐卤做豆腐 |
| B、在河流入海处易形成沙洲 |
| C、“尿毒症”患者做血液透析治疗 |
| D、三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 |
向10mL0.1mol?L-1NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL,下列叙述正确的是( )
| A、x=10时,溶液中有NH4+、Al3+、SO42-,且c( NH4+)>c(Al3+) |
| B、x=15时,溶液中有NH4+、SO42-,且c(NH4+)<2c(SO42-) |
| C、x=20时,溶液中有NH4+、Al3+、OH-,且c(OH-)<c(Al3+) |
| D、x=30时,溶液中有Ba2+、AlO2-、OH-,且c(OH-)=c(Ba2+) |
25℃时,水的电离达到平衡,下列叙述正确的是( )
| A、向水中加入少量NaOH,平衡逆向移动,新平衡时c(OH-)降低 |
| B、向水中加入少量NH4Cl,平衡正向移动,新平衡时c(OH-)降低 |
| C、pH=5的醋酸和pH=9的氨水中由水电离出的c(OH-)不相等 |
| D、将水加热,Kw增大,pH不变 |

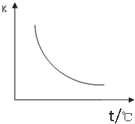 工业上制备H2的一种重要方法是:CO( g)+H2 O(g)?CO2(g)+H2(g)△H=Q kJ/mol.已知该反应的平衡常数 K 与温度的关系如图所示.若在一固定的密闭容器中,850℃时发生上述反应,并测得容器内各物质 的浓度(mol?L-1)随时间的变化关系如表:
工业上制备H2的一种重要方法是:CO( g)+H2 O(g)?CO2(g)+H2(g)△H=Q kJ/mol.已知该反应的平衡常数 K 与温度的关系如图所示.若在一固定的密闭容器中,850℃时发生上述反应,并测得容器内各物质 的浓度(mol?L-1)随时间的变化关系如表: