题目内容
丹尼尔?舍特曼是2011年诺贝尔化学奖获得者.他第一个发现了准晶体(准晶体晶体是一种介于晶体和非晶体之间的固体物质).科学研究发现.三种金属或两种金属可以组成准晶体.现有铁、铜和铝组成的准晶体样品M.某研究性学习小组.为了探究准晶体样品M的组成及含量.拟定了以下探究过程.清回答下列问题:
【实验目标】
探究准晶体样品M的成分及含量.
【提出假设】
猜想l:样品M的成分是铁和铜:
情想2:样品M的成分是铁和铝;
猜想3:样品M的成分足铜和铝;
猜想4(请你补充)
【设计实验】
取两份质量均为mg的样品M.按实验1(如图1所示)和实验2(如图2所示.图2的C管是碱式滴定管)装置进行实验:
实验前后都是常温、常压.按图1、图2实验方案都能顺利完成实验.待样品M完全溶解后.测得气体体积析算成标准状况下分别为V1mL和V2mL.
(1)写出实验1锥形瓶中可能发生反应的离子方程式 .
(2)实验2装置的气密性检验的操作方法是 .
【实验数据处理】
(3)若V2>V1≠0,则样品M的组成是 .
(4)若猜想2成立,则样品M中铁的质量分数为 .
【实验评价】
(5)实验l的装置(图1)和实验2的装置(图2)均能实现固体和液体反应产生气体.并都能测得产生气体的体积.甲同学认为实验1的装置(图1)比实验2的(图2)更好.乙同学认为实验2的装置(图2)比实验1的装置(图1)更好.请你简述乙同学的理由是 (任写一条)

【实验目标】
探究准晶体样品M的成分及含量.
【提出假设】
猜想l:样品M的成分是铁和铜:
情想2:样品M的成分是铁和铝;
猜想3:样品M的成分足铜和铝;
猜想4(请你补充)
【设计实验】
取两份质量均为mg的样品M.按实验1(如图1所示)和实验2(如图2所示.图2的C管是碱式滴定管)装置进行实验:
实验前后都是常温、常压.按图1、图2实验方案都能顺利完成实验.待样品M完全溶解后.测得气体体积析算成标准状况下分别为V1mL和V2mL.
(1)写出实验1锥形瓶中可能发生反应的离子方程式
(2)实验2装置的气密性检验的操作方法是
【实验数据处理】
(3)若V2>V1≠0,则样品M的组成是
(4)若猜想2成立,则样品M中铁的质量分数为
【实验评价】
(5)实验l的装置(图1)和实验2的装置(图2)均能实现固体和液体反应产生气体.并都能测得产生气体的体积.甲同学认为实验1的装置(图1)比实验2的(图2)更好.乙同学认为实验2的装置(图2)比实验1的装置(图1)更好.请你简述乙同学的理由是

考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:据题意,M只含铁、铝、铜三种金属中的两种或三种,所以猜想4:M的成分是铜、铁、铝;其中铝既能与强酸反应,又能与强碱反应;铁只能溶于强酸,不溶于强碱;铜既不溶于氢氧化钠,也不溶于稀硫酸.
(1)实验1中氢氧化钠溶液只与铝反应;
(2)检验该装置气密性的操作方法为:关闭分液漏斗旋塞,向量气管中注入水,使量气管内的水面高于左边容器内的水面,静置,若水面不发生变化,则装置气密性好;
(3)根据铝既能与强酸反应,又能与强碱反应;铁只能溶于强酸,不溶于强碱;铜既不溶于氢氧化钠,也不溶于稀硫酸,若V2>V1≠0,说明样品M的组成是一定含有铁和铝,可能含有铜;
(4)若猜想2成立,即样品M的成分是铁和铝,根据V2-V1即为铁与盐酸反应生成的氢气计算铁的量,再进一步计算含量;
(5)根据实验2的装置(图2)的特点量气更准确 或 调平液面更方便 或 不易堵塞等来分析.
(1)实验1中氢氧化钠溶液只与铝反应;
(2)检验该装置气密性的操作方法为:关闭分液漏斗旋塞,向量气管中注入水,使量气管内的水面高于左边容器内的水面,静置,若水面不发生变化,则装置气密性好;
(3)根据铝既能与强酸反应,又能与强碱反应;铁只能溶于强酸,不溶于强碱;铜既不溶于氢氧化钠,也不溶于稀硫酸,若V2>V1≠0,说明样品M的组成是一定含有铁和铝,可能含有铜;
(4)若猜想2成立,即样品M的成分是铁和铝,根据V2-V1即为铁与盐酸反应生成的氢气计算铁的量,再进一步计算含量;
(5)根据实验2的装置(图2)的特点量气更准确 或 调平液面更方便 或 不易堵塞等来分析.
解答:
解:据题意,M只含铁、铝、铜三种金属中的两种或三种,所以猜想4:M的成分是铜、铁、铝;其中铝既能与强酸反应,又能与强碱反应;铁只能溶于强酸,不溶于强碱;铜既不溶于氢氧化钠,也不溶于稀硫酸.
猜想4:M的成分是铜、铁、铝,故答案为:铜、铁、铝;
(1)实验1中氢氧化钠溶液只与铝反应,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)检验该装置气密性的操作方法为:关闭分液漏斗旋塞,向量气管中注入水,使量气管内的水面高于左边容器内的水面,静置,若水面不发生变化,则装置气密性好;故答案为:关闭分液漏斗旋塞,向量气管中注入水,使量气管内的水面高于左边容器内的水面,静置,若水面不发生变化,则装置气密性好;
(3)根据铝既能与强酸反应,又能与强碱反应;铁只能溶于强酸,不溶于强碱;铜既不溶于氢氧化钠,也不溶于稀硫酸,若V2>V1≠0,说明样品M的组成是一定含有铁和铝,可能含有铜,故答案为:一定含有铁和铝,可能含有铜;
(4)若猜想2成立,即样品M的成分是铁和铝,则V2-V1即为铁与盐酸反应生成的氢气,所以铁的质量为:
×10-3×56=0.0025(V2-V1),则样品M中铁的质量分数为
×100%=
×100%,故答案为:
×100%;
(5)实验2的装置(图2)相对于实验1的装置(图1)具有量气更准确或调平液面更方便或不易堵塞等优点,故答案为:量气更准确或调平液面更方便或不易堵塞等.
猜想4:M的成分是铜、铁、铝,故答案为:铜、铁、铝;
(1)实验1中氢氧化钠溶液只与铝反应,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)检验该装置气密性的操作方法为:关闭分液漏斗旋塞,向量气管中注入水,使量气管内的水面高于左边容器内的水面,静置,若水面不发生变化,则装置气密性好;故答案为:关闭分液漏斗旋塞,向量气管中注入水,使量气管内的水面高于左边容器内的水面,静置,若水面不发生变化,则装置气密性好;
(3)根据铝既能与强酸反应,又能与强碱反应;铁只能溶于强酸,不溶于强碱;铜既不溶于氢氧化钠,也不溶于稀硫酸,若V2>V1≠0,说明样品M的组成是一定含有铁和铝,可能含有铜,故答案为:一定含有铁和铝,可能含有铜;
(4)若猜想2成立,即样品M的成分是铁和铝,则V2-V1即为铁与盐酸反应生成的氢气,所以铁的质量为:
| V 2-V 1 |
| 22.4 |
| 0.0025(V2-V1) |
| m |
| V 2-V 1 |
| 400m |
| V 2-V 1 |
| 400m |
(5)实验2的装置(图2)相对于实验1的装置(图1)具有量气更准确或调平液面更方便或不易堵塞等优点,故答案为:量气更准确或调平液面更方便或不易堵塞等.
点评:本题考查了物质性质的分析判断,实验装置的理解应用,掌握基础是关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各组中的离子,能在水溶液中大量共存的是( )
| A、K+、H+、SO42-、OH- |
| B、Na+、Ca2+、CO32-、NO3- |
| C、Na+、H+、Cl-、CO32- |
| D、Na+、Cu2+、SO42-、Cl- |
在一定温度下的定容密闭容器中,当下列物理量不再变化时,表明反应:A(s)+2B(g)?C(g)+D(g)已达平衡的标志是( )
| A、混合气体的压强 |
| B、混合气体的密度 |
| C、容器内B、C、D的浓度之比为2:1:1 |
| D、混合气体的总物质的量 |
实验室需480mL 1.0mol/L的NaOH溶液,假如其他操作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是( )
| A、称取氢氧化钠20.0 g |
| B、定容时俯视观察刻度线 |
| C、移液时,对用于溶解氢氧化钠的烧杯没有进行冲洗 |
| D、移液用玻璃棒引流时,玻璃棒下端靠在容量瓶刻度线上方 |
有关下列物质分子结构特征描述正确的是( )
| A、乙烯分子中碳、氢原子个数比为1:2,证明乙烯分子里含有一个碳碳双键 |
B、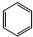 表示苯分子的结构,因此能解释邻二甲苯有 表示苯分子的结构,因此能解释邻二甲苯有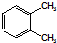 和 和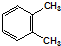 两种结构 两种结构 |
C、因为甲烷是一种正四面体结构,所以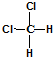 和 和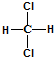 属于同一种物质 属于同一种物质 |
| D、苯的分子式是C6H6,分子式中碳原子远没有饱和,因此苯能使溴水褪色 |