题目内容
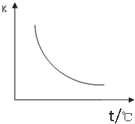 工业上制备H2的一种重要方法是:CO( g)+H2 O(g)?CO2(g)+H2(g)△H=Q kJ/mol.已知该反应的平衡常数 K 与温度的关系如图所示.若在一固定的密闭容器中,850℃时发生上述反应,并测得容器内各物质 的浓度(mol?L-1)随时间的变化关系如表:
工业上制备H2的一种重要方法是:CO( g)+H2 O(g)?CO2(g)+H2(g)△H=Q kJ/mol.已知该反应的平衡常数 K 与温度的关系如图所示.若在一固定的密闭容器中,850℃时发生上述反应,并测得容器内各物质 的浓度(mol?L-1)随时间的变化关系如表:| 时间/min | CO(g) | H2O | CO2 | H2(g) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.238 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C1 | C1 |
| 4 | C1 | C2 | C1 | C1 |
(1)下列可以判断该反应达到化学平衡状态的是
A.单位时间内减少 CO(g)的浓度等于生成 CO2 (g)的浓度
B.反应容器内的压强不发生变化
C.混合气体中 H2 (g)的浓度不再发生改变
D.氢气的生成速率等于水的消耗速率
(2)Q
(3)若在850℃时向反应容器中充入H2O(g),K 值
(4)上表中C2为
考点:化学平衡状态的判断,化学平衡的计算
专题:化学平衡专题
分析:(1)A.任何时候,正反应速率之比等于化学计量数之比;
B.反应前后气体的物质的量不变,温度一定,容器中压强始终不变;
C.反应达到平衡状态时,各物质的浓度不变;
D.氢气的生成速率等于水的消耗速率,正逆反应速率相等;
(2)由图可知,温度越高平衡常数越小,说明升高温度平衡向逆反应移动,据此判断△H;
(3)平衡常数只与温度有关,增大水的浓度,平衡正向移动,增大CO的转化率;
(4)根据三段式解题法,求出反应混合物各组分浓度的变化量、平衡时各组分的浓度,转化率=
×100%.
B.反应前后气体的物质的量不变,温度一定,容器中压强始终不变;
C.反应达到平衡状态时,各物质的浓度不变;
D.氢气的生成速率等于水的消耗速率,正逆反应速率相等;
(2)由图可知,温度越高平衡常数越小,说明升高温度平衡向逆反应移动,据此判断△H;
(3)平衡常数只与温度有关,增大水的浓度,平衡正向移动,增大CO的转化率;
(4)根据三段式解题法,求出反应混合物各组分浓度的变化量、平衡时各组分的浓度,转化率=
| CO的浓度变化 |
| CO的起始浓度 |
解答:
解:(1)A.任何时候,单位时间内减少CO(g)的浓度等于生成CO2(g)的浓度,不能说明到达平衡,故A错误;
B.反应前后气体的物质的量不变,温度一定,容器中压强始终不变,所以压强不发生变化,不能说明到达平衡,故B错误;
C.反应达到平衡状态时,各物质的浓度不变,说明到达平衡状态,故C正确;
D.任何时候,氢气的生成速率等于水的消耗速率,不能说明到达平衡状态,故D错误;
故选:C;
(2)由图可知,温度越高平衡常数越小,说明升高温度平衡向逆反应移动,升高温度平衡向吸热反应移动,故△H<0,故答案为:<;
(3)在850℃时向反应容器中充入H2O(g),平衡正向移动,但K值不变;增大水的浓度,平衡正向移动,增大CO的转化率,故答案为:不变;增大CO的转化率;
(4)CO+H2O(g)?CO2 +H2,
起始(mol/L) 0.200 0.300 0 0
反应(mol/L) a a a a
平衡(mol/L) 0.200-a 0.300-a a a
k=[CO
=
=1,解得a=0.12,
所以c2=0.300-a=0.18,CO(g)的转化率为
×100%=
×100%=60%,
故答案为:0.18;60%.
B.反应前后气体的物质的量不变,温度一定,容器中压强始终不变,所以压强不发生变化,不能说明到达平衡,故B错误;
C.反应达到平衡状态时,各物质的浓度不变,说明到达平衡状态,故C正确;
D.任何时候,氢气的生成速率等于水的消耗速率,不能说明到达平衡状态,故D错误;
故选:C;
(2)由图可知,温度越高平衡常数越小,说明升高温度平衡向逆反应移动,升高温度平衡向吸热反应移动,故△H<0,故答案为:<;
(3)在850℃时向反应容器中充入H2O(g),平衡正向移动,但K值不变;增大水的浓度,平衡正向移动,增大CO的转化率,故答案为:不变;增大CO的转化率;
(4)CO+H2O(g)?CO2 +H2,
起始(mol/L) 0.200 0.300 0 0
反应(mol/L) a a a a
平衡(mol/L) 0.200-a 0.300-a a a
k=[CO
| [CO2]?[H2] |
| [CO]?[H2O] |
| a×a |
| (0.200-a)?(0.300-a) |
所以c2=0.300-a=0.18,CO(g)的转化率为
| CO的浓度变化 |
| CO的起始浓度 |
| 0.12 |
| 0.200 |
故答案为:0.18;60%.
点评:本题考查化学平衡常数及影响因素、平衡移动、平衡状态的判断以及计算等,难度中等,注意平衡状态的判断,选择的物理量随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列物质属于电解质的是( )
| A、S |
| B、Cl2 |
| C、NaOH |
| D、CH4 |
下列关于电离平衡常数(K)的说法正确的是( )
| A、不同浓度的同一弱电解质,其电离平衡常数(K)不同 |
| B、电离平衡常数(K)越小,表示弱电解质电离能力越弱 |
| C、多元弱酸各步电离平衡常数相互关系为:K1<K2<K3 |
| D、CH3COOH溶液中加入少量CH3COONa溶液,电离常数减小 |
某研究性小组在CO还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X,他们认为X不一定只有是Fe,因为加热温度不同,受热不均时会含有少量的Fe3O4为探究X的成分及含量,他们进行了如图所示实验.下列有关叙述中正确的是( )
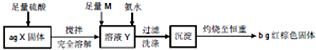

| A、取少量溶液Y,加入KSCN溶液,如果溶液不变红,则X中不含Fe3O4 | ||
| B、向钾氨水后得溶液中滴加FeCl2,如果生成红褐色沉淀,说明氨水已过量 | ||
| C、m可以是H2O2或NaClO,在实验过程中,理论上消耗两者物质的量之比为1;2 | ||
D、当b<
|
实验室需480mL 1.0mol/L的NaOH溶液,假如其他操作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是( )
| A、称取氢氧化钠20.0 g |
| B、定容时俯视观察刻度线 |
| C、移液时,对用于溶解氢氧化钠的烧杯没有进行冲洗 |
| D、移液用玻璃棒引流时,玻璃棒下端靠在容量瓶刻度线上方 |
有一部分潮解和变质的氢氧化钠样品W g(即含水和碳酸钠)),将其加入到100mL2mol?L-1的稀H2SO4中充分反应后,再加入20g 20%的NaOH溶液,恰好得到中性溶液,则蒸干此中性溶液可得固体的质量为( )
| A、14.2g |
| B、19.6g |
| C、28.4g |
| D、30.4g |
 影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究.实验药品:铜、铁、镁、0.5mol/LH2SO4、2mol/LH2SO4、18.4mol/LH2SO4
影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究.实验药品:铜、铁、镁、0.5mol/LH2SO4、2mol/LH2SO4、18.4mol/LH2SO4