题目内容
19.食盐和工业用盐具有广泛的用途.已知工业用盐主要成分为NaNO2,外观酷似食盐并有咸味.NaNO2有氧化性和还原性,遇酸分解放出NO2.(1)下列试剂可鉴别工业用盐和食盐的是bc.
a.H2O b.硝酸酸化的硝酸银 c.盐酸
(2)NaNO2与氢碘酸反应(含氮产物为NO)的离子方程式为2NO2-+2I-+4H+=I2+2NO↑+2H2O.
(3)某工厂废液中含有2%~5%的NaNO2,直接排放会造成水污染,但加入下列物质中的某一种就能使NaNO2中的氮转化为对空气无污染的气体,该物质是b.
a.NaCl b.NH4Cl c.浓H2SO4
(4)氯碱工业通过电解饱和食盐水来获得相应的产物.请写出电解食盐水的离子方程式2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-,
若在标准状况下生成3.36L H2,则溶液中生成的OH-的物质的量为0.3mol.
分析 (1)根据Cl-的特征反应,可用硝酸酸化的硝酸银鉴别,根据NaNO2遇酸分解放出NO2,可用盐酸鉴别;
(2)根据NO2-的氧化性和I-的还原性,可以写出NO2-与HI反应的离子方程式;
(3)使NaNO2中的氮转化为对空气无污染的气体(氮气),需要另一种反应物具有还原性,只有NH4Cl符合;
(4)根据2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑可知n(OH-)=2n(H2)=0.3 mol.
解答 解:(1)根据Cl-的特征反应,可用硝酸酸化的硝酸银鉴别,根据NaNO2遇酸分解放出NO2,可用盐酸鉴别,故选:bc;
(2)根据NO2-的氧化性和I-的还原性,可以写出NO2-与HI反应生成碘单质和一氧化氮,所以离子方程式为2NO2-+2I-+4H+=I2+2NO↑+2H2O,故答案为:2NO2-+2I-+4H+=I2+2NO↑+2H2O;
(3)因NaNO2转化为不引起污染的N2的过程中N的化合价降低,另一物质化合价必升高,
故答案为:b;
(4)电解食盐水的离子方程式为2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-;标准状况下生成3.36L H2,所以$\frac{3.36L}{22.4L/mol}$=0.15mol,而n(OH-)=2n(H2)=0.15mol×2=0.3 mol,故答案为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-;0.3 mol.
点评 本题主要结合亚硝酸盐考查了氧化还原反应的知识,考查的方式比较灵活,能较好的体现学生运用知识的能力.

练习册系列答案
相关题目
9.下列操作,没有考虑反应速率的是( )
| A. | 酸性KMnO4与H2C2O4溶液反应时,加入少量的MnSO4 | |
| B. | Zn与H2SO4溶液反应时,加入少的CuSO4晶体 | |
| C. | Cu 丝与浓H2SO4溶液反应时,将Cu丝做成螺旋状 | |
| D. | 铁丝能与水蒸气反应,不与冷水反应 |
10.根据表格中所给的相关数据回答问题
(1)SiCl4的晶体类型是分子晶体;碳化铝的晶体类型是原子晶体.
(2)能否用电解熔融AlCl3的方法来制取铝?为什么?不能(填能或否),理由是AlCl3是分子晶体,熔融时不能导电.
| NaCl | AlCl3 | SiCl4 | 碳化铝 | |
| 熔点 | 810℃ | 190℃ | -68℃ | 2200℃ |
(2)能否用电解熔融AlCl3的方法来制取铝?为什么?不能(填能或否),理由是AlCl3是分子晶体,熔融时不能导电.
7.在标准状况下进行甲、乙、丙三组实验.三组实验均各取30mL同浓度的盐酸,加入同一种镁铝合金粉末,产生气体,有关数据见下表:
(1)甲、乙两组实验中,哪一组盐酸是不足量的?乙(填“甲”或“乙”).理由是因甲反应后的溶液中再加合金还能继续反应,说明甲中盐酸有剩余,若乙中盐酸恰好完全反应或有剩余,则产生的氢气应为$\frac{280}{255}$385mL=423mL>336mL,故说明乙中盐酸不足.
(2)依据题中数据计算出盐酸的物质的量浓度,求得的盐酸的物质的量浓度为1mol/L.
(3)依据题中数据求合金中Mg、Al的物质的量之比,求得的Mg、Al物质的量之比为1:1.
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 生成气体体积/mL | 280 | 336 | 336 |
(2)依据题中数据计算出盐酸的物质的量浓度,求得的盐酸的物质的量浓度为1mol/L.
(3)依据题中数据求合金中Mg、Al的物质的量之比,求得的Mg、Al物质的量之比为1:1.
14.下列物质与危险化学品标志的对应关系正确的是( )
| A. |  乙醇 | B. |  金属钠 | C. |  天然气 | D. |  乙酸 |
8.下列化学反应中,属于氧化还原反应的是( )
| A. | Na2CO3+CaCl2═CaCO3↓+2NaCl | B. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O | ||
| C. | Fe+CuSO4═Cu+FeSO4 | D. | CaO+H2O═Ca(OH)2 |
 磷单质及其化合物在工业上有广泛应用.磷最重要的矿物资源是磷灰石,磷灰石主要有氟 磷灰石和羟基磷灰石.氟磷灰石在高温下制备白磷的化学方程式为:4Ca5 (P04)3F+21Si02+30C═3P4+20CaSi03+30CO+SiF4,结合上述反应中涉及到的物质或元素回答相关问题:
磷单质及其化合物在工业上有广泛应用.磷最重要的矿物资源是磷灰石,磷灰石主要有氟 磷灰石和羟基磷灰石.氟磷灰石在高温下制备白磷的化学方程式为:4Ca5 (P04)3F+21Si02+30C═3P4+20CaSi03+30CO+SiF4,结合上述反应中涉及到的物质或元素回答相关问题: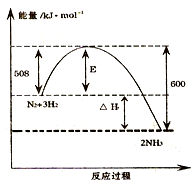 如图表示了298K时氮气与氢气合成氨反应过程中的能量变化,据此请回答:
如图表示了298K时氮气与氢气合成氨反应过程中的能量变化,据此请回答: 2NH3(g)△H=-92kJ/mol.
2NH3(g)△H=-92kJ/mol.