题目内容
15.下列实验的失败原因可能是因为缺少必要的实验步骤造成的是( )①将乙醇和乙酸混合,再加入稀硫酸共热制乙酸乙酯
②实验室用无水乙醇和浓硫酸共热到140℃制乙烯
③验证某RX是碘代烷,把RX与烧碱水溶液混合加热后,将溶液冷却后再加入硝酸银溶液出现褐色沉淀
④做醛的还原性实验时,当加入新制的氢氧化铜悬浊液后,未出现红色沉淀
⑤检验淀粉已经水解,将淀粉与少量稀硫酸加热一段时间后,加入银氨溶液后未析出银镜.
| A. | ③④⑤ | B. | ①③④⑤ | C. | ①④⑤ | D. | ④⑤ |
分析 ①制取乙酸乙酯用浓硫酸作催化剂;
②实验室用无水乙醇和浓硫酸共热到170℃制乙烯;
③卤代烃中卤元素检验时,应该先加稀硝酸后加硝酸银溶液;
④做醛的还原性实验时,当加入新制的氢氧化铜悬浊液后应该加热才能发生氧化反应;
⑤检验淀粉已经水解的葡萄糖时,应该先加NaOH后加银氨溶液.
解答 解:①制取乙酸乙酯用浓硫酸作催化剂而不是稀硫酸作催化剂,不缺少必要的实验步骤,故不选;
②实验室用无水乙醇和浓硫酸共热到170℃制乙烯,在140℃得到乙醚,不是缺少必要的实验步骤,故不选;
③卤代烃中卤元素检验时,应该先加稀硝酸后加硝酸银溶液,否则硝酸银和NaOH反应而得不到AgI沉淀,所以是缺少必要的实验步骤,故选;
④做醛的还原性实验时,当加入新制的氢氧化铜悬浊液后应该加热才能发生氧化反应,否则不发生反应,所以缺少必要的实验步骤,故选;
⑤检验淀粉已经水解的葡萄糖时,应该先加NaOH后加银氨溶液,否则银氨溶液和稀硫酸反应而干扰实验,所以缺少必要的实验步骤,故选;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及实验步骤及实验操作,明确实验原理及实验基本操作方法是解本题关键,注意银镜反应、卤代烃中卤元素检验时反应条件,为易错点.

练习册系列答案
相关题目
5.明•于谦诗:“凿开混沌得乌金,藏蓄阳和意最深.爝火燃回春浩浩,洪炉照破夜沉沉.”这里“乌金”指的是( )
| A. | 煤 | B. | 磁铁矿 | C. | 石油 | D. | 金 |
6.用NA表示阿伏加德罗常数,下列有关说法正确的是( )
| A. | 2.0g D218O中含有的质子数为NA | |
| B. | 标准状况下,22.4L NH3分子含有的杂化轨道数为4NA | |
| C. | 78g Na2O2晶体中所含阴、阳离子个数均为2NA | |
| D. | 1mol Fe完全溶于一定量的硝酸溶液中,转移的电子数一定是3NA |
3.布洛芬片常用来减轻普通感冒或流行性感冒引起的发热.布洛芬结构简式如图.下列说法错误的是( )
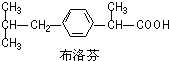

| A. | 布洛芬的分子式C13H18O2 | |
| B. | 布洛芬与苯乙酸(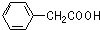 )是同系物 )是同系物 | |
| C. | 布洛芬苯环上的一氯代物有2种 | |
| D. | 常温条件下,1 mol布洛芬完全与金属钠反应可得到1 mol H2 |
10.镁片和锌片用导线连接后插入稀硫酸中,锌片是( )
| A. | 比镁片活泼 | B. | 电子流出极 | C. | 正极 | D. | 负极 |
2.要鉴别己烯中是否混有少量甲苯,最好的方法是( )
| A. | 先加入足量的高锰酸钾溶液,然后再加溴水 | |
| B. | 加入浓硫酸和浓硝酸后再加热 | |
| C. | 先加入足量的溴水,然后再加入高锰酸钾酸性溶液 | |
| D. | 点燃这种液体,然后再观察火焰的明亮程度 |
9.环丙烷可作为全身麻醉剂,环己烷是重要的有机溶剂.下面是部分环烷烃及烷烃衍生物的结构简式、键线式和某些有机化合物的反应式(其中Pt、Ni是催化剂且催化性能相当)

回答下列问题:
(1)环烷烃与相同碳原子数的烯烃(或相对分子质量相同的烯烃)是同分异构体.
(2)从反应①~③可以看出,最容易发生开环加成反应的环烷烃是环丙烷(填名称),判断依据为在都使用催化剂的条件下,加成反应的温度最低.
(3)环烷烃还可与卤素单质、卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件下反应,其化学方程式为 (不需注明反应条件)
(不需注明反应条件)
(4)写出鉴别环丙烷与丙烯的一种方法,试剂酸性高锰酸钾溶液;现象与结论使酸性高锰酸钾溶液退色的是丙烯,另一种是环丙烷(或溴水,使溴水退色的是丙烯).
(5)已知某烯烃在酸性高锰酸钾的作用下只产生一种有机物C3H6O,其产物物质的量是原烯烃的两倍且其氢核磁共振谱图上只有一个峰,则该烯烃的结构简式为C(CH3)2=C(CH3)2,系统名称为2,3-二甲基-2-丁烯.
| 结构简式 |  |  | Br-CH2-CH2-CH(CH3)-CH2-Br |
| 键线式 |  (环己烷) (环己烷) |  (环丁烷) (环丁烷) |  |

回答下列问题:
(1)环烷烃与相同碳原子数的烯烃(或相对分子质量相同的烯烃)是同分异构体.
(2)从反应①~③可以看出,最容易发生开环加成反应的环烷烃是环丙烷(填名称),判断依据为在都使用催化剂的条件下,加成反应的温度最低.
(3)环烷烃还可与卤素单质、卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件下反应,其化学方程式为
 (不需注明反应条件)
(不需注明反应条件)(4)写出鉴别环丙烷与丙烯的一种方法,试剂酸性高锰酸钾溶液;现象与结论使酸性高锰酸钾溶液退色的是丙烯,另一种是环丙烷(或溴水,使溴水退色的是丙烯).
(5)已知某烯烃在酸性高锰酸钾的作用下只产生一种有机物C3H6O,其产物物质的量是原烯烃的两倍且其氢核磁共振谱图上只有一个峰,则该烯烃的结构简式为C(CH3)2=C(CH3)2,系统名称为2,3-二甲基-2-丁烯.
7.下列实验中,对应的方法或现象以及结论都正确的是( )
| 选项 | 实验 | 方法或现象 | 结论 |
| A | 检查该装置气密性: | 将注射器针管向右拉动一段距离后松手,能够恢复原位 | 气密性良好 |
| B | 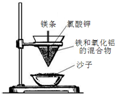 | 点燃镁条后,火花四射,在蒸发皿中产生红热的金属 | 铝热反应: 2Fe+Al2O3$\frac{\underline{\;高温\;}}{\;}$2Al+Fe2O3 |
| C | 将SO2气体通入氢硫酸溶液中 | 有黄色浑浊产生 | 还原性:H2S>SO2 |
| D | 制备CuSO4 | 方法一:用Cu与浓硫酸反应 方法二:用Cu与稀硫酸在不断通入O2的情况下反应 | 方法二更符合绿色化学理念 方法一的原子利用率更高 |
| A. | A | B. | B | C. | C | D. | D |
