题目内容
10.镁片和锌片用导线连接后插入稀硫酸中,锌片是( )| A. | 比镁片活泼 | B. | 电子流出极 | C. | 正极 | D. | 负极 |
分析 根据镁片和锌片用导线连接插入稀硫酸中构成原电池,则活泼的金属镁为负极,镁失去电子发生氧化反应,不活泼的锌为正极,氢离子在正极得到电子发生还原反应,据此分析.
解答 解:镁片和锌片用导线连接插入稀硫酸中构成原电池,则活泼的金属镁为负极,镁失去电子发生氧化反应,不活泼的锌为正极,氢离子在正极得到电子发生还原反应.
A.根据金属活动顺序表知在酸中镁片比锌片活泼,故A错误;
B.活泼的金属镁为负极,镁失去电子,沿导线流入正极,即锌片,故B错误;
C.不活泼的锌为正极,发生还原反应,反应式为2H++2e-=H2↑,故C正确;
D.不活泼的锌为正极,发生还原反应,故D错误;
故选C.
点评 本题考查了原电池工作原理中正负极的判断知识,根据活泼的金属镁为负极发生氧化反应,不活泼的锌为正极发生还原反应,较简单.

练习册系列答案
相关题目
2.下列叙述正确的是( )
| A. | 淀粉、蛋白质、油脂均是天然高分子化合物 | |
| B. | 铜矿石在细菌作用下可直接转化为单质铜,这个过程叫生物炼铜 | |
| C. | 氟氯烃的肆意排放会加速臭氧层的破坏,使大气层中的紫外线增强 | |
| D. | 凯库勒的“基团理论”尽管存在缺陷,但仍对有机化学的发展起到了巨大的推动作用 |
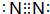 ,Z的原子结构示意图
,Z的原子结构示意图 .
.
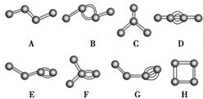 如图表示4个碳原子相互结合的方式.小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合.
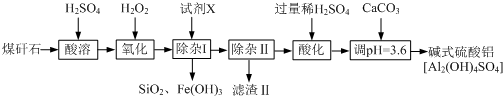
如图表示4个碳原子相互结合的方式.小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合. 小明和同班同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
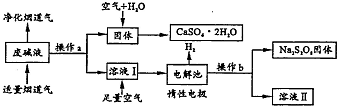
小明和同班同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验. 为了充分应用资源,用工业废碱液(Ca(OH)2、NaOH)与烟道气(回收成份SO2)来制取石膏(CaSO4•2H2O)和过二硫酸钠(Na2S2O8).设计简要流程如下:
为了充分应用资源,用工业废碱液(Ca(OH)2、NaOH)与烟道气(回收成份SO2)来制取石膏(CaSO4•2H2O)和过二硫酸钠(Na2S2O8).设计简要流程如下: