题目内容
6.用NA表示阿伏加德罗常数,下列有关说法正确的是( )| A. | 2.0g D218O中含有的质子数为NA | |
| B. | 标准状况下,22.4L NH3分子含有的杂化轨道数为4NA | |
| C. | 78g Na2O2晶体中所含阴、阳离子个数均为2NA | |
| D. | 1mol Fe完全溶于一定量的硝酸溶液中,转移的电子数一定是3NA |
分析 A、求出D218O的物质的量,然后根据1molD218O中含12个质子来分析;
B、求出氨气的物质的量,然后根据1mol氨气中含4mol杂化轨道来分析;
C、求出过氧化钠的物质的量,然后根据1mol氧化钠中含2mol钠离子和1mol过氧根来分析;
D、铁和硝酸反应后的最终价态可能是+3价,还可能是+2价.
解答 解:A、2.0gD218O的物质的量n=$\frac{2g}{22g/mol}$=$\frac{1}{11}$mol,而1molD218O中含12个质子,故$\frac{1}{11}$molD218O中含$\frac{12}{11}{N}_{A}$个质子,故A错误;
B、标况下22.4L氨气的物质的量为1mol,而1mol氨气中含4mol杂化轨道,故含4NA个杂化轨道,故B正确;
C、78g过氧化钠的物质的量为1mol,而1mol氧化钠中含2mol钠离子和1mol过氧根,故含3NA个离子,故C错误;
D、铁和硝酸反应后的最终价态可能是+3价,还可能是+2价,故1mol铁转移的电子数不一定是3NA个,还可能是2NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
17.CoCl2•6H20是一种陶瓷着色剂.利用水钴矿[主要成分为Co203、Co(OH)3,还含少量Fe203、Al203、MnO等]制取CoCl2•6H20的工艺流程如图1:

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH如表:(金属离子浓度为:0.01mol/L)
③CoCl2•6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴.
(1)写出浸出过程中Co(OH)3发生反应的离子方程式2Co(OH)3+SO32-+4H+=2Co2++SO42-+5H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O.
(3)“加Na2CO3调pH至a”,则a的范围是5.2≤PH<7.6.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解;
(5)萃取剂对金属离子的萃取率与pH的关系如图2.向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+;其使用的最佳pH范围是B.
A.2.0〜2.5 B.3.0〜3.5 C.4.0〜4.5 D.5.0〜5.5
(6)操作1为蒸发浓缩、冷却结晶、过滤.
(7)实验室用足量的浓盐酸完全溶解一定量的钴的氧化物Cox0y(其中钴的化合价为+2、+3),若得到含13gCoCl2的溶液并产生标准状况下448mL的黄绿色气体,则y:x=6:5.

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH如表:(金属离子浓度为:0.01mol/L)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co(OH)3发生反应的离子方程式2Co(OH)3+SO32-+4H+=2Co2++SO42-+5H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O.
(3)“加Na2CO3调pH至a”,则a的范围是5.2≤PH<7.6.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解;
(5)萃取剂对金属离子的萃取率与pH的关系如图2.向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+;其使用的最佳pH范围是B.
A.2.0〜2.5 B.3.0〜3.5 C.4.0〜4.5 D.5.0〜5.5
(6)操作1为蒸发浓缩、冷却结晶、过滤.
(7)实验室用足量的浓盐酸完全溶解一定量的钴的氧化物Cox0y(其中钴的化合价为+2、+3),若得到含13gCoCl2的溶液并产生标准状况下448mL的黄绿色气体,则y:x=6:5.
14.NA为阿伏加罗常数的值,下列叙述正确的是( )
| A. | 1molCH3+中含有的电子数为10NA | |
| B. | 1mol铁粉与1mol水蒸气充分反应转移的电子数为3A | |
| C. | 0.1mol/L的Al2(SO4)3溶液中,Al3+的数目小于0.2NA | |
| D. | 电解精炼铜时,若转移了NA个电子,则阴极析出32g铜 |
11.磷石膏是磷氨厂生产硫酸和磷酸所排放的废渣(主要成分为CaSO4•2H2O),大量堆积既占用土地,又易造成环境污染和硫资源的浪费,所以可从资源综合利用的角度将磷石膏转化成硫酸钾和氯化钙晶体,工艺流程如下:
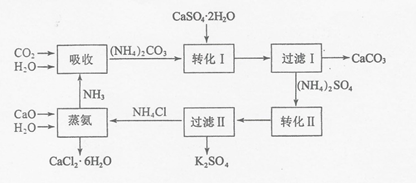
请回答以下问题:
(1)为了提高原料的利用率,吸收流程中通入CO2和NH3的先后顺序最好为先通入NH3,后通入CO2.
(2)碳酸铵溶液与磷石膏悬浊溶液混合后发生转化I的离子反应方程式为CaSO4+CO32-?CaCO3+SO42.
(3)工艺流程中除了所给出的CaCO3、CaSO4•2H2O、NH3、H2O等原料外,在转化Ⅱ的过程中还需要加入KCl原料.
(4)①过滤Ⅱ后所得滤液NH4Cl溶液,确认其中含有Cl-的方法是:取滤液少量与试管中,滴加足量的硝酸钡或氢氧化钡至无沉淀生成,静置后取上层清夜少量与另一支试管中,滴加稀硝酸至溶液呈酸性后,再滴加硝酸银溶液,如果有白色沉淀生成,即可证明原滤液中含有氯离子;
②氯化钙结晶水合物(CaCl2•6H2O)是目前常用的无机储热材料,选择的依据是因为ad(选填序号);
A.熔点较低(29℃熔化) b.能导电 c.能制冷 d.无毒
③已知不同温度下K2SO4在100g水中达到饱和时溶解的量如下表:
60℃时K2SO4的饱和溶液945.6g冷却到0℃,可析出K2SO4晶体86.4g.
(5)上述工艺流程中循环利用的物质是NH3;还有一种物质,只要其纯净,也可以被循环利用,它是CaCO3(均填化学式).

请回答以下问题:
(1)为了提高原料的利用率,吸收流程中通入CO2和NH3的先后顺序最好为先通入NH3,后通入CO2.
(2)碳酸铵溶液与磷石膏悬浊溶液混合后发生转化I的离子反应方程式为CaSO4+CO32-?CaCO3+SO42.
(3)工艺流程中除了所给出的CaCO3、CaSO4•2H2O、NH3、H2O等原料外,在转化Ⅱ的过程中还需要加入KCl原料.
(4)①过滤Ⅱ后所得滤液NH4Cl溶液,确认其中含有Cl-的方法是:取滤液少量与试管中,滴加足量的硝酸钡或氢氧化钡至无沉淀生成,静置后取上层清夜少量与另一支试管中,滴加稀硝酸至溶液呈酸性后,再滴加硝酸银溶液,如果有白色沉淀生成,即可证明原滤液中含有氯离子;
②氯化钙结晶水合物(CaCl2•6H2O)是目前常用的无机储热材料,选择的依据是因为ad(选填序号);
A.熔点较低(29℃熔化) b.能导电 c.能制冷 d.无毒
③已知不同温度下K2SO4在100g水中达到饱和时溶解的量如下表:
| 温度(℃) | 0 | 20 | 60 |
| K2SO4溶解的量(g) | 7.4 | 11.1 | 18.2 |
(5)上述工艺流程中循环利用的物质是NH3;还有一种物质,只要其纯净,也可以被循环利用,它是CaCO3(均填化学式).
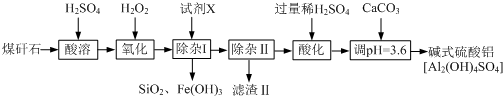
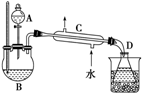 乙醇的沸点是78℃,能与水以任意比混溶,易与氯化钙结合生成配合物.乙醚的沸点为34,.6℃,难溶于水,乙醚极易燃烧.实验室制乙醚的反应原理是2CH3CH2OH$→_{140℃}^{浓H_{2}SO_{4}}$CH3CH2-O-CH2CH3(乙醚)+H2O
乙醇的沸点是78℃,能与水以任意比混溶,易与氯化钙结合生成配合物.乙醚的沸点为34,.6℃,难溶于水,乙醚极易燃烧.实验室制乙醚的反应原理是2CH3CH2OH$→_{140℃}^{浓H_{2}SO_{4}}$CH3CH2-O-CH2CH3(乙醚)+H2O