题目内容
3.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 标准状况下,11.2 L CCl4中含有的分子数为0.5NA | |
| B. | 在Na2O2与水的反应中,每生成1 mol O2,转移电子的数为2NA | |
| C. | 常温常压下,7.8 g苯中含有双键的数目为0.3NA | |
| D. | 25℃时,0.1 mol•L-1 NH4NO3溶液中含有的铵根离子数为0.1NA |
分析 A、标况下四氯化碳为液体;
B、过氧化钠和水的反应中,氧元素的价态由-1价变为0价;
C、苯不是单双键交替的结构;
D、溶液体积不明确.
解答 解:A、标况下四氯化碳为液体,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、过氧化钠和水的反应中,氧元素的价态由-1价变为0价,故当生成1mol氧气时转移2NA 个电子,故B正确;
C、苯不是单双键交替的结构,即苯中无碳碳双键,故C错误;
D、溶液体积不明确,故溶液中的铵根离子的个数无法计算,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
13.化学与生活密切相关,下列有关说法错误的是( )
| A. | Al(OH)3是某些胃药的一种成分 | |
| B. | 乳酸铁是某些补铁口服液的有效成分 | |
| C. | 臭氧可以作为新型自来水消毒剂 | |
| D. | SO2常用作红葡萄酒中杀菌消毒剂 |
11.用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮水处理的新技术,制取Na2FeO4的反应为:Fe2O3+3Na2O2=2Na2FeO4+Na2O,下列说法不正确的是( )
| A. | Fe2O3是反应的还原剂 | |
| B. | Na2O2既是氧化剂又是还原剂 | |
| C. | Na2FeO4是反应的氧化产物 | |
| D. | 氧化剂与还原剂的物质的量的比是3:1 |
8.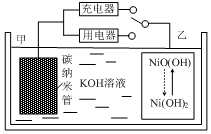 2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )
2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )
 2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )
2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )| A. | 放电时,甲电极为正极,OH-移向乙电极 | |
| B. | 放电时,乙电极反应为:NiO(OH)+H2O+e-=Ni(OH)2+OH- | |
| C. | 充电时,电池的碳电极与直流电源的正极相连 | |
| D. | 电池总反应为H2+2NiOOH$?_{充电}^{放电}$2Ni(OH)2 |
5.为减轻大气污染,可在汽车尾气排放处加装催化转化装置,反应方程式为:2NO(g)+2CO(g)$?_{△}^{催化剂}$2CO2(g)+N2(g).
(1)上述反应使用等质量的某种催化剂时,温度和催化剂的比表面积对化学反应速率的影响对比实验如下表,c(NO)浓度随时间(t)变化曲线如图:
①表中a=1.20×10-3.
②实验说明,该反应是放热反应(填“放热”或“吸热”).
③若在500℃时,投料$\frac{{c({NO})}}{{c({CO})}}=1$,NO的转化率为80%,则此温度时的平衡常数K=第一种情况:设c(NO)=1mol•L-1,则K=160,
第二种情况:设c(NO)=amol•L-1,K=$\frac{160}{a}$,
第三种情况:设n(NO)=amol,容器的容积为V L,则K=$\frac{160V}{a}$.
(2)使用电化学法也可处理NO的污染,装置如图2.已知电解池阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:2HSO3-+2H++2e-=S2O42-+2H2O.吸收池中除去NO的离子方程式为:2NO+2S2O42-+2H2O=N2+4HSO3-.
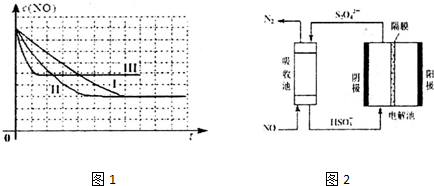
(1)上述反应使用等质量的某种催化剂时,温度和催化剂的比表面积对化学反应速率的影响对比实验如下表,c(NO)浓度随时间(t)变化曲线如图:
| 编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | a | 5.80×10-3 | 124 |
| Ⅲ | 350 | 1.20×10-3 | 5.80×10-3 | b |
②实验说明,该反应是放热反应(填“放热”或“吸热”).
③若在500℃时,投料$\frac{{c({NO})}}{{c({CO})}}=1$,NO的转化率为80%,则此温度时的平衡常数K=第一种情况:设c(NO)=1mol•L-1,则K=160,
第二种情况:设c(NO)=amol•L-1,K=$\frac{160}{a}$,
第三种情况:设n(NO)=amol,容器的容积为V L,则K=$\frac{160V}{a}$.
(2)使用电化学法也可处理NO的污染,装置如图2.已知电解池阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:2HSO3-+2H++2e-=S2O42-+2H2O.吸收池中除去NO的离子方程式为:2NO+2S2O42-+2H2O=N2+4HSO3-.




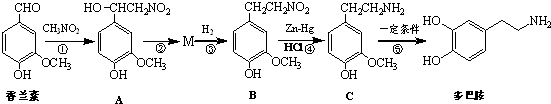
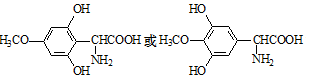 .
.