题目内容
4.某学生用0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:(A)移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)BDCEAF.
(2)上述(B)操作的目的是防止将标准液稀释.
(3)上述(A)操作之前,如先用待测液润洗锥形瓶,则对测定结果的影响是(填偏大、偏小、不变,下同)偏大.
(4)实验中用左手控制滴定管活塞(填仪器及部位),眼睛注视锥形瓶中溶液的颜色变化,直至滴定终点.判断到达终点的现象是锥形瓶中溶液的颜色由无色变浅红且保持30秒内不褪色.
分析 (1)中和滴定有检漏、洗涤、润洗、装液、滴定等操作;
(2)滴定管在装液时,为了防止溶液被稀释,需用待装液润洗;
(3)根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析误差;
(4)实验中应控制流速并观察锥形瓶中颜色变化;如溶液颜色变化且半分钟内不变色,可说明达到滴定终点.
解答 解:(1)中和滴定按照检漏、洗涤、润洗、装液、取待测液并加指示剂、滴定等顺序操作,则正确的顺序为BDCEAF,
故答案为:BDCEAF;
(2)上述(B)操作的目的是防止将标准液稀释,
故答案为:防止将标准液稀释;
(3)上述(A)操作之前,如先用待测液润洗锥形瓶,待测液的物质的量偏大,则消耗的标准液体积偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,可知c(待测)偏大;
故答案为:偏大;
(4)滴定时,滴定过程中,用左手控制碱式滴定管橡皮管玻璃珠处,右手摇动锥形瓶,两眼应该注视锥形瓶内溶液的颜色变化;滴定时,锥形瓶中溶液的颜色由无色变浅红且保持30秒内不褪色,可说明达到滴定终点;
故答案为:滴定管活塞;锥形瓶中溶液的颜色变化;锥形瓶中溶液的颜色由无色变浅红且保持30秒内不褪色.
点评 本题考查酸碱中和滴定实验,题目难度不大,注意把握实验的步骤、方法以及注意事项,在误差分析时根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析即可.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
15.亚硫酸钠和硫粉通过化合反应可制得硫代硫酸钠(Na2S2O3).
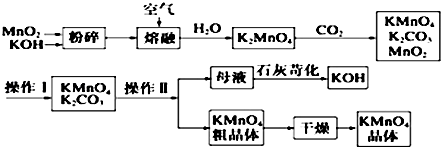
已知:Na2S2O3在酸性溶液中不能稳定存在.有关物质的溶解度随温度变化曲线如图2所示.某研究小组设计了制备Na2S2O3•5H2O的装置图(如图1).
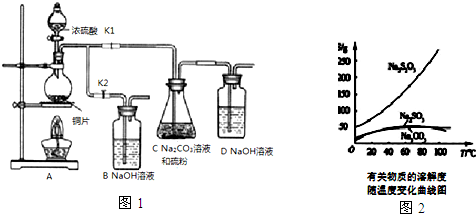
部分操作步骤如下:
①打开K1,关闭K2,向圆底烧瓶中加入足量浓硫酸,加热.
②C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.当C中溶液的pH接近7时,即停止C中的反应,停止加热
③过滤C中的混合液,并将滤液进行处理,得到产品.
(1)步骤①中,圆底烧瓶中发生反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)步骤②中,“当C中溶液的pH接近7时即停止C中的反应”的原因是Na2S2O3在酸性溶液中不能稳定存在.“停止C中的反应”的操作是打开K2,关闭K1.
(3)步骤③中,“过滤”用到的玻璃仪器是烧杯、漏斗、玻璃棒(填仪器名称).将滤液进行处理过程是将滤液经过加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.
依据反应2S2O32-+I2→S4O62-+2I-,可用I2的标准溶液测定产品的纯度.取5.5g产品配制成100mL溶液.取10mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,相关数据记录如表所示.
(4)判断达到滴定终点的现象是加入最后一滴I2标准溶液后,溶液变蓝,且半分钟不改变.
(5)Na2S2O3•5H2O在产品中的质量分数是90.2%.(计算结果请用百分数表示并保留1位小数)(Na2S2O3•5H2O的式量为248)
已知:Na2S2O3在酸性溶液中不能稳定存在.有关物质的溶解度随温度变化曲线如图2所示.某研究小组设计了制备Na2S2O3•5H2O的装置图(如图1).

部分操作步骤如下:
①打开K1,关闭K2,向圆底烧瓶中加入足量浓硫酸,加热.
②C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.当C中溶液的pH接近7时,即停止C中的反应,停止加热
③过滤C中的混合液,并将滤液进行处理,得到产品.
(1)步骤①中,圆底烧瓶中发生反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)步骤②中,“当C中溶液的pH接近7时即停止C中的反应”的原因是Na2S2O3在酸性溶液中不能稳定存在.“停止C中的反应”的操作是打开K2,关闭K1.
(3)步骤③中,“过滤”用到的玻璃仪器是烧杯、漏斗、玻璃棒(填仪器名称).将滤液进行处理过程是将滤液经过加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.
依据反应2S2O32-+I2→S4O62-+2I-,可用I2的标准溶液测定产品的纯度.取5.5g产品配制成100mL溶液.取10mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,相关数据记录如表所示.
| 编号 | 1 | 2 | 3 | 4 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.99 | 19.98 | 17.13 | 20.03 |
(5)Na2S2O3•5H2O在产品中的质量分数是90.2%.(计算结果请用百分数表示并保留1位小数)(Na2S2O3•5H2O的式量为248)
16.下列叙述正确的是( )
| A. | 化学反应必然伴随着能量的变化 | |
| B. | 能量转化的途径不同时,体系包含的总能量不同 | |
| C. | 放热反应指生成物的总能量高于反应物的总能量 | |
| D. | 吸热反应不加热就不会发生 |
13.某次采集酸雨样品,每隔一段时间测定一次pH,得到数据如表:
(1)放置时,雨水样品pH变化的主要原因酸雨样品中的H2SO3逐渐被氧化成H2SO4,使溶液的酸性增强.
(2)pH变化的离子方程式:2H2SO3+O2=4H++SO42-.
| 时间 | 开始 | 8小时 | 16小时 | 24小时 | 32小时 | 40小时 | 48小时 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
(2)pH变化的离子方程式:2H2SO3+O2=4H++SO42-.
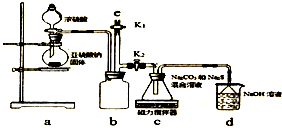 天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染.
天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染.