题目内容
11.下列说法中错误的是( )| A. | 氯气是一种黄绿色、有刺激性气味的气体 | |
| B. | 氯气、液氯和氯水是同一种物质 | |
| C. | 氯气能溶于水 | |
| D. | 氯气是一种有毒的气体,可用NaOH溶液吸收 |
分析 A、氯气是有颜色和刺激性气味的气体;
B、根据氯气、液氯和氯水的成分判断;
C、氯气是能溶于水的气体;
D、氯气是有毒气体,与氢氧化钠反应生成氯化钠和次氯酸钠.
解答 解:A、氯气是一种黄绿色、有刺激性气味的气体,故A正确;
B、液氯是氯气的液态,所以氯气和液氯是同一种物质;部分氯气和水反应生成盐酸和次氯酸,所以氯水中含有氯气分子、盐酸、次氯酸,是一种混合物,液氯和氯气与氯水不是同一种物质,故B错误;
C、氯气能溶于水,1体积的水能溶解2体积的氯气,故C正确;
D、氯气吸入后与粘膜和呼吸道的水作用形成氯化氢和新生态氧;氯化氢可使上呼吸道粘膜炎性水肿、充血和坏死; 新生态氧对组织具有强烈的氧化作用,并可形成具细胞原浆毒作用的臭氧;所以氯气是一种有毒的气体,可用NaOH溶液吸收,故D正确;
故选B.
点评 本题考查了氯气的性质,明确氯水中的成分有哪些,各种成分有什么性质,可用哪些实验验证.

练习册系列答案
相关题目
2.某化合物6.4g在氧气中完全燃烧,只生成8.8gCO2和5.4gH2O.下列说法正确的是( )
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:2 | ||
| C. | 该有机物的分子式为C2H6 | D. | 该化合物中一定含有氧元素 |
19.在天平的两个托盘上,分别放上质量相等的两只烧杯,在烧杯中分别加入同组成、同体积的稀硫酸(过量),此时天平呈平衡状态,然后分别向两只烧杯中加入等质量的碳酸钠和碳酸氢钠,反应终止后,天平( )
| A. | 放Na2CO3的一端重 | B. | 两端仍平衡 | ||
| C. | 放NaHCO3的一端重 | D. | 无法判断 |
6.在一定条件下,将m体积NO和n体积O2同时倒立于水中且盛满水的容器,充分反应后,容器内残留0.5m 体积的气体,该气体与空气接触后变为红棕色.则m与n的比值为( )
| A. | 3:2 | B. | 2:3 | C. | 8:3 | D. | 3:8 |
16.下列设计的实验方案能达到实验目的是( )
| A. | 检验蔗糖是否水解:蔗糖溶液在稀硫酸存在下水浴加热一段时间后,再与银氨溶液混合加热,观察现象 | |
| B. | 检验溶液中是否含有NH4+:取少量待检验溶液,向其中加入浓NaOH溶液加热,再用湿润的红色石蕊试纸放置试管口,观察现象 | |
| C. | 提纯含有少量苯酚的苯:向含有少量苯酚的苯加入过量浓溴水,振荡后静置过滤,除去三溴苯酚沉淀 | |
| D. | 探究化学反应的限度:取5mL0.1mol/LKI溶液,滴加0.1mol/LFeCl3溶液5~6滴,充分反应,根据溶液中是否含有碘单质和碘离子判断该反应有一定限度 |
3.已知下列反应的热化学方程式为
(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ•mol-1
(2)C(s)+O2(g)═CO2(g)△H2=-393.5kJ•mol-1
(3)H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H3=-285.8kJ•mol-1
则反应2C(s)+2H2(g)+O2(g)═CH3COOH(l)的△H为( )
(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ•mol-1
(2)C(s)+O2(g)═CO2(g)△H2=-393.5kJ•mol-1
(3)H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H3=-285.8kJ•mol-1
则反应2C(s)+2H2(g)+O2(g)═CH3COOH(l)的△H为( )
| A. | -488.3 kJ•mol-1 | B. | -191 kJ•mol-1 | ||
| C. | -476.8 kJ•mol-1 | D. | -1 549.6 kJ•mol-1 |
20.碳酸亚乙酯是锂离子电池低温电解液的重要添加剂,其结构如图.下列有关该物质的说法不正确的是( )

| A. | 分子式为C3H2O3 | |
| B. | 分子中σ键与π键个数之比为3:1 | |
| C. | 分子中既有极性键也有非极性键 | |
| D. | 分子中碳原子的杂化方式全部为sp2杂化 |
1.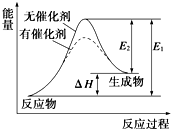 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A. | 该反应为放热反应 | |
| B. | 该反应的反应热等于E1-E2 | |
| C. | 催化剂能改变该反应的焓变 | |
| D. | 逆反应的活化能大于正反应的活化能 |