题目内容
1.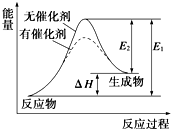 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A. | 该反应为放热反应 | |
| B. | 该反应的反应热等于E1-E2 | |
| C. | 催化剂能改变该反应的焓变 | |
| D. | 逆反应的活化能大于正反应的活化能 |
分析 A.图象分析反应物能量低于生成物能量,反应是吸热反应;
B.图象分析反应焓变=E1-E2;
C.催化剂对反应的焓变无影响;
D.E1是正反应的活化能,E2是逆反应的活化能,△H是反应的焓变.
解答 解:A.图象分析反应物能量低于生成物能量,反应是吸热反应,故A错误;
B.△H=断键吸收的能量-成键放出的能量=E1-E2,故B正确;
C.催化剂对反应的始态和终态无响应,只改变活化能,则对反应的焓变无影响,故C错误;
D.图象分析逆反应的活化能E2小于正反应的活化能E1,故D错误;
故选B.
点评 本题考查了化学变化过程中能量变化的分析的,主要是活化能概念的理解应用,掌握图象分析方法是关键,题目较简单.

练习册系列答案
相关题目
11.下列说法中错误的是( )
| A. | 氯气是一种黄绿色、有刺激性气味的气体 | |
| B. | 氯气、液氯和氯水是同一种物质 | |
| C. | 氯气能溶于水 | |
| D. | 氯气是一种有毒的气体,可用NaOH溶液吸收 |
9.某硝酸盐R(NO3)2受热分解为RO、NO2、O2,在标准状况下,将生成的气体充满一烧瓶,并将烧瓶倒置于水中,当烧瓶中液面不再上升时烧瓶内溶液浓度是( )
| A. | $\frac{4}{5}$mol•L-1 | B. | $\frac{1}{14}$mol•L-1 | C. | $\frac{1}{22.4}$mol•L-1 | D. | $\frac{1}{28}$mol•L-1 |
16.下列有关说法正确的是( )
| A. | 氨水稀释后,溶液中 的值减小 的值减小 | |
| B. | 0.1mol•L-1Na2CO3溶液加蒸馏水稀释,CO32-的水解程度增大,溶液的pH减小 | |
| C. | 电解精炼铜过程中,阳极质最的减少与阴极质量的增加一定相等 | |
| D. | 298K时,2H2S(g)+SO2(g)=3S(s)+2H2O(l)能自发进行,则其△H<0 |
6.己知反应:①PbO2+4HCI═PbCl2+C12↑+2H20,②Cu+2Fe3+═Cu2++2Fe2+,③Cl2+2Fe2+═2Cl-+2Fe3+.则有关物质(离子)的氧化性由强到弱的顺序为( )
| A. | Cl2>Fe3+>Cu2+>PbO2 | B. | PbO2>Cl2>Fe3+>Cu2+ | ||
| C. | Fe3+>Cu2+>PbO2>Cl2 | D. | Cu2+>Fe3+>Cl2>PbO2 |
10.用石墨电极电解下列物质的水溶液,两极都有气体生成且电解过程中溶液PH增大的是( )
| A. | KI | B. | H2SO4 | C. | NaOH | D. | Na2SO4 |
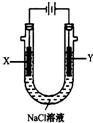
11.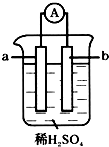 已知在金属活动性顺序表中,a为排在氢前面的金属.在如图所示的装置中,b为碳棒,关于此装置的各种叙述中,不正确的是( )
已知在金属活动性顺序表中,a为排在氢前面的金属.在如图所示的装置中,b为碳棒,关于此装置的各种叙述中,不正确的是( )
 已知在金属活动性顺序表中,a为排在氢前面的金属.在如图所示的装置中,b为碳棒,关于此装置的各种叙述中,不正确的是( )
已知在金属活动性顺序表中,a为排在氢前面的金属.在如图所示的装置中,b为碳棒,关于此装置的各种叙述中,不正确的是( )| A. | 碳棒上有气体放出,溶液酸性变弱 | B. | a是正极,b是负极 | ||
| C. | 导线中有电子从a极到b极 | D. | a极上发生了氧化反应 |
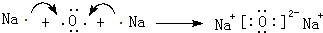 、
、 .
.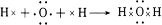 、
、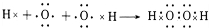 .
. 甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,甲醚可作燃料电池的燃料.
甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,甲醚可作燃料电池的燃料.