题目内容
20.碳酸亚乙酯是锂离子电池低温电解液的重要添加剂,其结构如图.下列有关该物质的说法不正确的是( )
| A. | 分子式为C3H2O3 | |
| B. | 分子中σ键与π键个数之比为3:1 | |
| C. | 分子中既有极性键也有非极性键 | |
| D. | 分子中碳原子的杂化方式全部为sp2杂化 |
分析 A.根据结构简式确定分子式;
B.双键中含有一个σ键、一个π键,单键都是σ键;
C.同种非金属元素之间形成非极性键,不同非金属元素之间形成极性键;
D.该分子C-O中C原子价层电子对个数是4且不含孤电子对、C=O中C原子价层电子对个数是3且不含孤电子对,根据价层电子对互斥理论判断C原子杂化方式.
解答 解:A.根据结构简式确定分子式为C3H2O3,故A正确;
B.双键中含有一个σ键、一个π键,单键都是σ键,所以该分子中含有10个σ键、1个π键,所以分子中σ键与π键个数之比为10:1,故B错误;
C.同种非金属元素之间形成非极性键,不同非金属元素之间形成极性键,所以C-之间存在非极性键、C-H和C-O原子之间存在极性键,故C正确;
D.该分子C-O中C原子价层电子对个数是4且不含孤电子对,C原子为sp3杂化;C=O中C原子价层电子对个数是3且不含孤电子对,C原子杂化方式为sp2,故D错误;
故选BD.
点评 本题考查物质结构,为高频考点,涉及原子杂化方式判断、化学键判断、分子式确定等知识点,侧重考查学生分析判断能力,难点是判断C原子杂化类型,题目难度不大.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
11.下列说法中错误的是( )
| A. | 氯气是一种黄绿色、有刺激性气味的气体 | |
| B. | 氯气、液氯和氯水是同一种物质 | |
| C. | 氯气能溶于水 | |
| D. | 氯气是一种有毒的气体,可用NaOH溶液吸收 |
8.下列关于NH4Fe(SO4)2溶液中离子浓度关系的说法中正确的是( )
| A. | 2c(SO42-)+c(OH-)=c(NH4+)+3c(Fe3+)+c(H+) | B. | c(NH4+)=c(Fe3+) | ||
| C. | c(NH4+)=$\frac{1}{2}$c(SO42-) | D. | c(OH-)>c(H+) |
15.下列化合物中含有手性碳原子的是( )
| A. | CCl2F2 | B. | 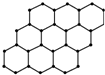 | C. | CH3CH2OH | D. | 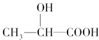 |
5.下列各组物质中,化学键类型完全相同的是( )
| A. | HI和NaI | B. | H2O2和CO2 | C. | Cl2和CCl4 | D. | MgCl2和NaBr |
9.某硝酸盐R(NO3)2受热分解为RO、NO2、O2,在标准状况下,将生成的气体充满一烧瓶,并将烧瓶倒置于水中,当烧瓶中液面不再上升时烧瓶内溶液浓度是( )
| A. | $\frac{4}{5}$mol•L-1 | B. | $\frac{1}{14}$mol•L-1 | C. | $\frac{1}{22.4}$mol•L-1 | D. | $\frac{1}{28}$mol•L-1 |
10.用石墨电极电解下列物质的水溶液,两极都有气体生成且电解过程中溶液PH增大的是( )
| A. | KI | B. | H2SO4 | C. | NaOH | D. | Na2SO4 |
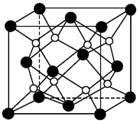 (1)原子序数小于36的X、Y、Z、W四种元素,其中X是元素周期表中原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.回答下列问题:
(1)原子序数小于36的X、Y、Z、W四种元素,其中X是元素周期表中原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.回答下列问题: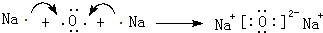 、
、 .
.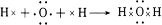 、
、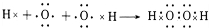 .
.