题目内容
18.室温下,将10mLpH=3的醋酸溶液加水稀释后,下列说法不正确是( )| A. | 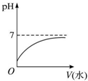 | |
| B. | 溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$不变 | |
| C. | 溶液中导电粒子的数目增加 | |
| D. | 再加入10 mL pH=11的NaOH溶液,恰好完全中和 |
分析 A.酸加水稀释时,溶液的pH逐渐接近7;
B.Kh为水解常数,只与温度有关;
C.在醋酸溶液中加水稀释,促进电离;
D.醋酸的浓度大于溶液中氢离子的浓度.
解答 解:A.加水稀释时,电离程度增大,但溶液的体积增大的倍数大于n(H+)增加的倍数,则c(H+)减小,溶液的pH逐渐接近7,但不能等于7,故A正确;
B.溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$=Kh,Kh为水解常数,只与温度有关,所以该值不变,故B正确;
C.醋酸是弱酸,存在电离平衡.在醋酸溶液中加水稀释,促进电离,则液中导电粒子的数目增多,故C正确;
D.等体积10mLpH=3的醋酸与pH=11的NaOH溶液混合时,醋酸的浓度大于0.001mol/L,二者反应时醋酸过量,故D错误.
故选D.
点评 本题考查弱电解质稀释的有关判断,主要是考查学生对弱电解质电离平衡特点以及外界条件对电离平衡影响的熟悉了解程度,答题明确温度与平衡常数的关系、溶液的pH与物质的量浓度的关系、稀释中溶液体积的变化与离子的物质的量的变化程度是解答本题的关键.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
19.已知氮气和氧气发生化合反应的能量变化图象如图所示.下列推断正确的是( )
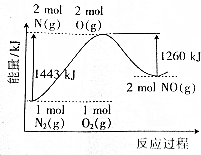

| A. | 氮气和氧气的反应是氧化还原反应,也是放热反应 | |
| B. | 1molNO分子被拆成原子要放出630kJ能量 | |
| C. | 1molN2(g)和1molO2(g)完全反应生成2molNO(g)时吸收183kJ能量 | |
| D. | 在酒精灯加热条件下,N2和O2能发生化合反应生成NO |
6.下列叙述中,能说明乙酸的酸性比碳酸强的是( )
| A. | 乙酸具有挥发性 | B. | 乙酸是一元酸 | ||
| C. | 乙酸是有机酸而碳酸是无机酸 | D. | 乙酸能与碳酸氢钠反应放出CO2 |
13. 某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,pH值随溶液体积变化的曲线如图所示.据图判断正确的是( )
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,pH值随溶液体积变化的曲线如图所示.据图判断正确的是( )
 某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,pH值随溶液体积变化的曲线如图所示.据图判断正确的是( )
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,pH值随溶液体积变化的曲线如图所示.据图判断正确的是( )| A. | 水电离程度d<a<b<c | |
| B. | b点溶液的导电性比c点溶液的导电性弱 | |
| C. | a点KW的数值比c点KW的数值大 | |
| D. | b点酸的总浓度大于a点酸的总浓度 |
3.室温下向10mL pH=11的稀氨水溶液中加入水稀释后,下列说法正确的是( )
| A. | 溶液中导电粒子的数目增加,导电性增强 | |
| B. | 氨水的电离程度增大,[OH-]减小 | |
| C. | 再加入10mL pH=3 HCl溶液,混合液pH=7 | |
| D. | 溶液中由水电离出的[OH-]=1×10-3 mol•L-1 |
10. 常温下有下列四种溶液:
常温下有下列四种溶液:
已知该温度下醋酸的电离平衡常数Ka=1.8×10-5.
请回答下列问题:
(1)用④的标准液滴定③宜选用酚酞(填“石蕊”、“酚酞”或“四基橙”)作为指示剂,①和②两种溶液中由水电离出的c(H+)之比为106:1,
(2)都是0.1mol/L的①NH4Cl②NH4HCO3③CH3COONH4 ④NH4HSO4的溶液中NH4+离子浓度大小顺序为④>①>③>②.(用序号填空)
(3)取溶液③滴定20mL溶液④,滴定曲线如图所示,则a点时溶液中各离子浓度的大小关系为c(Na+)>c(OH-)>c(CH3COO-)>c(H+);若b点时消耗③的体积为V mL,则V>20(填“>”、“<”或“=”).
 常温下有下列四种溶液:
常温下有下列四种溶液:| 序号 | ① | ② | ③ | ④ |
| 溶液 | pH=4的NH4Cl溶液 | pH=4的盐酸 | 0.1mol•L-1的醋酸溶液 | 0.1mol•L-1的NaOH溶液 |
请回答下列问题:
(1)用④的标准液滴定③宜选用酚酞(填“石蕊”、“酚酞”或“四基橙”)作为指示剂,①和②两种溶液中由水电离出的c(H+)之比为106:1,
(2)都是0.1mol/L的①NH4Cl②NH4HCO3③CH3COONH4 ④NH4HSO4的溶液中NH4+离子浓度大小顺序为④>①>③>②.(用序号填空)
(3)取溶液③滴定20mL溶液④,滴定曲线如图所示,则a点时溶液中各离子浓度的大小关系为c(Na+)>c(OH-)>c(CH3COO-)>c(H+);若b点时消耗③的体积为V mL,则V>20(填“>”、“<”或“=”).
7.用固体样品配制一定物质的量浓度的溶液,需经过溶解、转移、定容、摇匀等操作.下列图示对应的操作不规范的是( )
| A. | 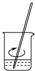 溶解 | B. |  转移 | C. |  定容 | D. | 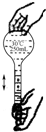 摇匀 |
 太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置.其材料除单晶硅,还有铜铟镓硒等化合物.
太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置.其材料除单晶硅,还有铜铟镓硒等化合物.