题目内容
7.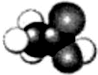 乙酸是食醋的主要成分,它的分子结构模型如图所示.
乙酸是食醋的主要成分,它的分子结构模型如图所示.(1)乙酸分子中-COOH原子团的名称是羧基.
(2)乙酸可使紫色石蕊溶液变红色.
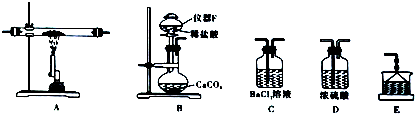
(3)一定条件下,乙酸能与乙醇发生反应生成一种具有香味的油状液体.某研究性学习小组成员分别设计了如下甲、乙、丙三套实验装置:
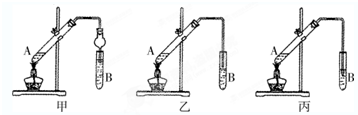
①甲、乙、丙三套装置中,不宜选用的装置是丙(填“甲”、“乙”、“丙”)
②乙酸与乙醇发生反应的化学方程式为CH3COOH+CH3CH2OH$?_{△}^{H_{2}SO_{4}}$CH3COOCH2CH3+H2O,该反应的类型是酯化(或取代)反应.
分析 (1)-COOH原子团的名称为羧基;
(2)乙酸显酸性,能使石蕊试液变红色;
(3)①吸收极易溶于水的气体时,若将导管伸入水中,由于气体溶于水,导致装置内压强急剧降低,外界大气压压着液体进入,产生倒吸现象;
②乙酸能与乙酸发生反应生成乙酸乙酯,为酯化反应,也属于取代反应.
解答 解:(1)乙酸是饱和一元羧酸,其-COOH原子团的名称为羧基;
故答案为:羧基;
(2)乙酸是一种有机酸,在溶液转化部分电离出氢离子,显酸性,能使石蕊试液变红色;
故答案为:红;
(3)①甲、乙、丙三套装置中,甲装置中,导管伸入吸收液中,并且连接了体积较大的容器,既能够防止倒吸,又能够很好的吸收乙酸乙酯中的乙酸和乙醇,乙装置中,将导管伸入液面上,能够很好的吸收乙酸乙酯中的乙酸和乙醇,可防止倒吸,丙装置中将导管伸入饱和碳酸钠溶液中,由于乙酸和乙醇溶于饱和碳酸钠溶液,导致装置内压强急剧降低,外界大气压压着液体进入,产生倒吸现象;
故答案为:丙;
②乙酸能与乙酸发生反应生成乙酸乙酯,该反应为CH3COOH+CH3CH2OH$?_{△}^{H_{2}SO_{4}}$CH3COOCH2CH3+H2O,为酯化反应,也属于取代反应,
故答案为:CH3COOH+CH3CH2OH$?_{△}^{H_{2}SO_{4}}$CH3COOCH2CH3+H2O;酯化(或取代).
点评 本题考查了乙酸乙酯的制备,题目难度不大,注意掌握乙酸与乙醇的反应原理及乙酸的化学性质,试题侧重基础知识的考查,有利于提高学生灵活应用基础知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.已知图一表示的是可逆反应CO(g)+H2(g)?C(s)+H2O(g)△H>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应N2O4(g)?2NO2(g)△H>0的浓度(c)随时间(t)的变化情况.下列说法中正确的是( )
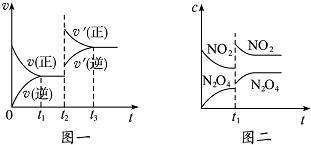

| A. | 图一t2时改变的条件可能是升高了温度或增大了压强 | |
| B. | 图一t2时改变的条件是增大压强,则反应的△H增大 | |
| C. | 图二t1时改变的条件可能是升高了温度 | |
| D. | 若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将增大 |
2.其他条件不变,升高温度下列数据不一定增大的是( )
| A. | 水的离子积常数KW | B. | 可逆反应的平衡常数K | ||
| C. | 0.1mol/LCH3COONa溶液的pH | D. | NH3•H2O的电离常数Kb |
17.取一定质量的均匀固体混合物Cu、Cu2O和CuO,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少3.20g,另一份加入1000mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体2.24L,则所用硝酸的物质的量浓度为( )
| A. | 0.8mol/L | B. | 1.6mol/L | C. | 0.9mol/L | D. | 1.8mol/L |

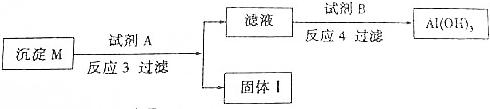
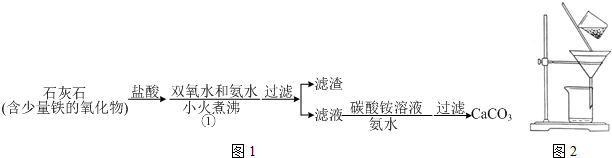
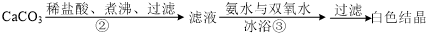
 如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5ml 饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答:
如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5ml 饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答: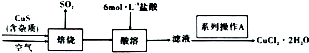
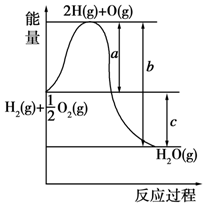 已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(g),反应过程中能量变化如图所示,请回答下列问题.
已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(g),反应过程中能量变化如图所示,请回答下列问题.