��Ŀ����
���������г��õ�����������������ᡱָ���ᡢ��������ᣬ�����ָ�ռ�ʹ��
��1�������ᡱ�롰���֮����ɷ�Ӧ�������ʱ�����û�ѧ����ʽ��ʾ���������������ӷ���ʽ��ʾȴֻ��������һ����H++OH-=H2O����д����һ�����ӷ���ʽ�� ��
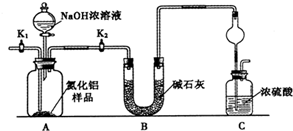
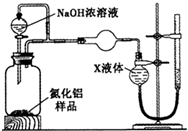
��2��ʵ�����Ʊ�H2��CO2��NH3��SO2ʱ���������ϡ������Ʊ�����ͬ������ ��
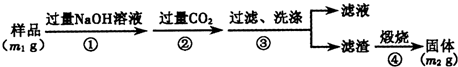
��3���ռ������Һ��������CO2������0.1mol NaOH����Һ����һ����CO2����Һ����С�����ɵõ��������ɿ���������������ֱ��ǣ��ѧʽ����
�� ��Na2CO3 ��Na2CO3��NaHCO3 ��NaHCO3��
��4������3���õ��Ĺ��������ܽ���ˮ�������м������ᣬ������Һ��pHǡ�õ���7���ٽ���Һ���ɣ����յõ����������Ϊ g��
��5�����ú�°��Ƽ���������һ�֣���д����ȡС�մ�ʱ����Һ�з�����Ӧ���ܻ�ѧ����ʽ ��
��1�������ᡱ�롰���֮����ɷ�Ӧ�������ʱ�����û�ѧ����ʽ��ʾ���������������ӷ���ʽ��ʾȴֻ��������һ����H++OH-=H2O����д����һ�����ӷ���ʽ��
��2��ʵ�����Ʊ�H2��CO2��NH3��SO2ʱ���������ϡ������Ʊ�����ͬ������
��3���ռ������Һ��������CO2������0.1mol NaOH����Һ����һ����CO2����Һ����С�����ɵõ��������ɿ���������������ֱ��ǣ��ѧʽ����
��
��4������3���õ��Ĺ��������ܽ���ˮ�������м������ᣬ������Һ��pHǡ�õ���7���ٽ���Һ���ɣ����յõ����������Ϊ
��5�����ú�°��Ƽ���������һ�֣���д����ȡС�մ�ʱ����Һ�з�����Ӧ���ܻ�ѧ����ʽ
���㣺���ӷ���ʽ����д,�ᡢ��Ρ�������ĸ�������ϵ,���Ļ�ѧ����,��������Ļ�ѧ����,�Ƶ���Ҫ������
ר�⣺Ԫ�ؼ��仯����
��������1��������ǿ�ᷴӦ���ɿ������Ρ�ˮ��������̼��
��2���������ϡ������Ʊ�������
��3����0.1mol NaOH����Һ����һ����CO2����2NaOH+CO2=Na2CO3+H2O��NaOH+CO2=NaHCO3���Դ˷�����
��4������3���õ��Ĺ��������ܽ���ˮ�������м������ᣬ������Һ��pHǡ�õ���7������ΪNaCl�������ԭ���غ���㣻
��5�����ñ����Ȼ�����Һ��������������̼��ȡ��ȡС�մ�
��2���������ϡ������Ʊ�������
��3����0.1mol NaOH����Һ����һ����CO2����2NaOH+CO2=Na2CO3+H2O��NaOH+CO2=NaHCO3���Դ˷�����
��4������3���õ��Ĺ��������ܽ���ˮ�������м������ᣬ������Һ��pHǡ�õ���7������ΪNaCl�������ԭ���غ���㣻
��5�����ñ����Ȼ�����Һ��������������̼��ȡ��ȡС�մ�
���
�⣺��1��������ǿ�ᷴӦ���ɿ������Ρ�ˮ��������̼�������ӷ�ӦΪCO32-+2H+=H2O+CO2�����ʴ�Ϊ��CO32-+2H+=H2O+CO2����
��2�����ý��������ᡢ���ᷴӦ�����Ʊ�H2���ʴ�Ϊ��H2��
��3����0.1mol NaOH����Һ����һ����CO2����2NaOH+CO2=Na2CO3+H2O��NaOH+CO2=NaHCO3�������ߵ����ʵ����ȴ���2��1��������̼���㣬��С�����ɵõ�����ΪNa2CO3��NaOH������2��1ʱ����ΪNa2CO3��1��1ʱ����ΪNaHCO3������2��2��2��1֮��ʱ����ΪNa2CO3��NaHCO3���ʴ�Ϊ��Na2CO3��NaOH��
��4������3���õ��Ĺ��������ܽ���ˮ�������м������ᣬ������Һ��pHǡ�õ���7������ΪNaCl������ԭ���غ��֪��NaCl������Ϊ0.1mol��58.5g/mol=5.85g��
�ʴ�Ϊ��5.85��
��5�������Ȼ�����Һ��������������̼��ȡ��ȡС�մ�ӦΪH2O+CO2+NaCl+NH3=NaHCO3��+NH4Cl���ʴ�Ϊ��H2O+CO2+NaCl+NH3=NaHCO3��+NH4Cl��
��2�����ý��������ᡢ���ᷴӦ�����Ʊ�H2���ʴ�Ϊ��H2��
��3����0.1mol NaOH����Һ����һ����CO2����2NaOH+CO2=Na2CO3+H2O��NaOH+CO2=NaHCO3�������ߵ����ʵ����ȴ���2��1��������̼���㣬��С�����ɵõ�����ΪNa2CO3��NaOH������2��1ʱ����ΪNa2CO3��1��1ʱ����ΪNaHCO3������2��2��2��1֮��ʱ����ΪNa2CO3��NaHCO3���ʴ�Ϊ��Na2CO3��NaOH��
��4������3���õ��Ĺ��������ܽ���ˮ�������м������ᣬ������Һ��pHǡ�õ���7������ΪNaCl������ԭ���غ��֪��NaCl������Ϊ0.1mol��58.5g/mol=5.85g��
�ʴ�Ϊ��5.85��
��5�������Ȼ�����Һ��������������̼��ȡ��ȡС�մ�ӦΪH2O+CO2+NaCl+NH3=NaHCO3��+NH4Cl���ʴ�Ϊ��H2O+CO2+NaCl+NH3=NaHCO3��+NH4Cl��
���������⿼�����ӷ�Ӧ����ʽ����д��Ϊ��Ƶ���㣬���շ����Ļ�ѧ��Ӧ�����ӷ�Ӧ����д����Ϊ���Ĺؼ������ظ��ֽⷴӦ�����ӷ�Ӧ������Ŀ��飬ע�ⷢ���ķ�Ӧ���غ㷨���㣬��Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ѧ���쳵��������������������ϵ�д�
ѧ���쳵��������������������ϵ�д�
�����Ŀ
�ܱ������У���ӦxA��g��+yB��g��?zC��g����ƽ��ʱ��A��Ũ��Ϊ0.5mol/L���������¶Ȳ��䣬���������ݻ�����ԭ����2��������ƽ��ʱA��Ũ�Ƚ�Ϊ0.3mol/L�������жϲ���ȷ���ǣ�������
| A��B��ת���ʽ��� |
| B��ƽ��������Ӧ�����ƶ� |
| C��x+y��z |
| D��C����������½� |
������Ϊ�У����ϰ�ȫҪ����ǣ�������
| A���Ͻ��ڼ���վ����ȼ���̻����� |
| B�������������Ż�ʱ��������մˮ��ë������ |
| C�����д�������й©ʱ����Ӧ��˳�緽����ɢ |
| D������������ķ�Һ����ˮ�أ��ô���ˮ������ˮ�� |
��һ���¶������£������Ѵﵽƽ��ķ�Ӧ��FeCl3+3KSCN?3KCl+Fe��SCN��3���ڴ���Һ�������´�����ƽ�����Ƶ��ǣ�������
| A�����������Ȼ��ع��� |
| B�����������Ȼ������� |
| C������Fe��SCN��3��Ũ�� |
| D����ˮϡ�� |
ͨ��NOx�������ɼ��NOx�ĺ������乤��ԭ��ʾ��ͼ���£�����˵������ȷ���ǣ�������

| A��Pt�缫�Ǹ�װ�õ����� |
| B���õ�ط�����������ӦΪ��O2+4e-+2H2O=4OH- |
| C�������ĵ缫��Ӧʽ��NO-2e-+O2-=NO2 |
| D������������O2-���ƶ� |
 �����б�������ˮ�����Ե����壬����ǿ�
�����б�������ˮ�����Ե����壬����ǿ� ������Ԫ����X��Y��R��Q��Ԫ�����ڱ��е�λ����ͼ��ʾ������QԪ���ǵؿ��к�����ߵ�Ԫ�أ�
������Ԫ����X��Y��R��Q��Ԫ�����ڱ��е�λ����ͼ��ʾ������QԪ���ǵؿ��к�����ߵ�Ԫ�أ�