题目内容
塑化剂是工业上被广泛使用的高分子材料助剂,在塑料加工中添加这种物质,可以使其柔韧性增强,容易加工.塑化剂可合法用于工业生产,但禁止作为食品添加剂.截止2011年6月8日,台湾被检测出含塑化剂食品已达961种,据媒体报道,2012年岁末,我国大陆多种著名品牌白酒也陷入了塑化剂风波.常见塑化剂为邻苯二甲酸酯类物质,某有机物J(C19H20O4)是一种塑料工业中常用的塑化剂,可用下列合成路线合成.

已知:Ⅰ.
Ⅱ.控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应;
Ⅲ.F与浓溴水混合不产生白色沉淀.
请回答下列问题:
(1)F中官能团的电子式为 .
(2)写出反应①④的化学反应方程式:反应① .反应④ .
(3)C4H10O的同分异构体中属于醇类的有多种,写出其中具有手性碳原子的同分异构体的结构简式: .
(4)以含碳原子数不同的苯的同系物为原料,可以合成不同种类的塑化剂.教材中苯及其同系物的通式是CnH2n-6(n≥6),某同学根据等差数列公式推导出该系列的通式却是Cn+5H2n+4,老师告诉该同学他推导出的通式也是正确的,但其中n的意义和取值范围与教材中的通式不同,请问:通式Cn+5H2n+4中n的意义是 .

已知:Ⅰ.

Ⅱ.控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应;
Ⅲ.F与浓溴水混合不产生白色沉淀.
请回答下列问题:
(1)F中官能团的电子式为
(2)写出反应①④的化学反应方程式:反应①
(3)C4H10O的同分异构体中属于醇类的有多种,写出其中具有手性碳原子的同分异构体的结构简式:
(4)以含碳原子数不同的苯的同系物为原料,可以合成不同种类的塑化剂.教材中苯及其同系物的通式是CnH2n-6(n≥6),某同学根据等差数列公式推导出该系列的通式却是Cn+5H2n+4,老师告诉该同学他推导出的通式也是正确的,但其中n的意义和取值范围与教材中的通式不同,请问:通式Cn+5H2n+4中n的意义是
考点:有机物的合成
专题:有机物的化学性质及推断
分析:D为苯的同系物,D与氯气反应生成E,E与NaOH的水溶液发生取代反应生成F,F与浓溴水混合不产生白色沉淀,则F为: 、E为
、E为 、D为
、D为 ;根据图示反应①为:
;根据图示反应①为: ,则A的结构简式为
,则A的结构简式为 ;反应④为:
;反应④为: +
+
 +H2O;控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应,则B为
+H2O;控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应,则B为 ;B与E(
;B与E( )发生反应生成J(
)发生反应生成J( ),据此进行解答.
),据此进行解答.
 、E为
、E为 、D为
、D为 ;根据图示反应①为:
;根据图示反应①为: ,则A的结构简式为
,则A的结构简式为 ;反应④为:
;反应④为: +
+
| 浓硫酸 |
| △ |
 +H2O;控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应,则B为
+H2O;控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应,则B为 ;B与E(
;B与E( )发生反应生成J(
)发生反应生成J( ),据此进行解答.
),据此进行解答.解答:
解:D为苯的同系物,D与氯气反应生成E,E与NaOH的水溶液发生取代反应生成F,F与浓溴水混合不产生白色沉淀,则F为: 、E为
、E为 、D为
、D为 ;根据图示反应①为:
;根据图示反应①为: ,则A的结构简式为
,则A的结构简式为 ;反应④为:
;反应④为: +
+
 +H2O;控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应,则B为
+H2O;控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应,则B为 ;B与E(
;B与E( )反应生成J(
)反应生成J( ),
),
(1)根据分析可知,F的结构简式为: ,F中官能团为-OH,羟基的电子式为
,F中官能团为-OH,羟基的电子式为 ,故答案为:
,故答案为: ;
;
(2)根据图示反应①的化学反应方程式为: ;
;
反应④的化学反应方程式是: +
+
 +H2O,
+H2O,
故答案为: ;
; +
+
 +H2O;
+H2O;
(3)C4H10O的同分异构体中属于醇类的有多种,其中具有手性碳原子的同分异构体的结构简式为:CH3CH2CH(OH)CH3,
故答案为:CH3CH2CH(OH)CH3;
(4)当n=1时,分子式为:C6H6,为苯,则在通式Cn+5H2n+4中n的意义是代表苯及其同系物这一系列中的第n项,
故答案为:代表苯及其同系物这一系列中的第n项.
 、E为
、E为 、D为
、D为 ;根据图示反应①为:
;根据图示反应①为: ,则A的结构简式为
,则A的结构简式为 ;反应④为:
;反应④为: +
+
| 浓硫酸 |
| △ |
 +H2O;控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应,则B为
+H2O;控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应,则B为 ;B与E(
;B与E( )反应生成J(
)反应生成J( ),
),(1)根据分析可知,F的结构简式为:
 ,F中官能团为-OH,羟基的电子式为
,F中官能团为-OH,羟基的电子式为 ,故答案为:
,故答案为: ;
;(2)根据图示反应①的化学反应方程式为:
 ;
;反应④的化学反应方程式是:
 +
+
| 浓硫酸 |
| △ |
 +H2O,
+H2O,故答案为:
 ;
; +
+
| 浓硫酸 |
| △ |
 +H2O;
+H2O;(3)C4H10O的同分异构体中属于醇类的有多种,其中具有手性碳原子的同分异构体的结构简式为:CH3CH2CH(OH)CH3,
故答案为:CH3CH2CH(OH)CH3;
(4)当n=1时,分子式为:C6H6,为苯,则在通式Cn+5H2n+4中n的意义是代表苯及其同系物这一系列中的第n项,
故答案为:代表苯及其同系物这一系列中的第n项.
点评:本题考查有机合成,题目难度中等,试题涉及有机物的结构、性质、相互转化、官能团的电子式、方程式和同分异构体的书写及通式的含义等知识,熟练掌握常见有机物结构与性质为解答关键,试题培养了学生的分析、理解能力.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、吸热反应在一定条件下也可以发生 |
| B、需要加热才能发生的反应不一定是吸热反应 |
| C、反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小 |
| D、放热反应在常温下一定很容易发生 |
将相同物质的量浓度的某弱酸HX与NaX溶液等体积混合,测得混合溶液中C(Na+)>C(X-),则下列关系错误的是( )
| A、C(OH-)<C(H+) |
| B、C(HX)>C(x-) |
| C、C(HX)+C(x-)=2C(Na+) |
| D、C(H+)+(Na+)=C(X-)+C(OH-) |



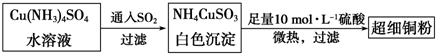

 常见的一硝基甲苯有对硝基甲苯和邻硝基甲苯两种,均可用于合成各种染料.某探究小组利用下列反应和装置制备一硝基甲苯.
常见的一硝基甲苯有对硝基甲苯和邻硝基甲苯两种,均可用于合成各种染料.某探究小组利用下列反应和装置制备一硝基甲苯.