��Ŀ����
4��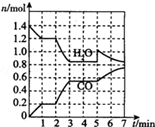 ��̿��CO��H2������Ҫ����Դ��Ҳ����Ҫ�Ļ���ԭ�ϣ�
��̿��CO��H2������Ҫ����Դ��Ҳ����Ҫ�Ļ���ԭ�ϣ���1����֪C��H2��CO��ȼ���ȣ���H���ֱ�Ϊ-393.5kJ•mol-1��-285.8kJ•mo
l-1��-283kJ•mol-1����֪ˮ��������Ϊ+44kJ/mol��
�ٽ�̿��ˮ������Ӧ����CO��H2���Ȼ�ѧ����ʽΪC��s��+H2O��g��=CO��g��+H2��g����H=+131.3kJ/mol
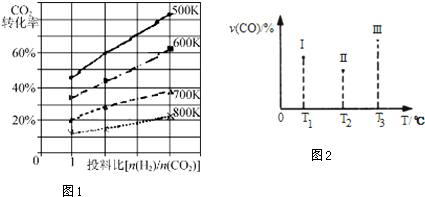
������������̿��2molˮ������ַ�Ӧ������������Ϊ191.7kJʱ�����ʱH2O��g����ת����Ϊ73%��
��2������̿��ˮ���������ݻ�Ϊ2L���ܱ������з�����Ӧ��
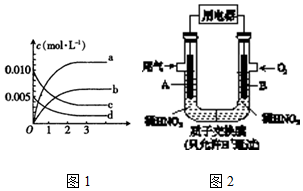
C��s��+H2O��g��?CO��g��+H2��g��������H2O��CO�����ʵ�����ʱ��ı仯������ͼ��ʾ��
�ٵ�һ��ƽ��ʱ�ε�ƽ�ⳣ����0.017��������2λ��Ч���֣�������Ӧ���е�2minʱ���ı����¶ȣ�ʹ���߷�����ͼ��ʾ�ı仯�����¶ȱ仯Ϊ���£�����¡����¡�����
�ڷ�Ӧ��5minʱ����Ҳֻ�ı���ijһ��������ʹ���߷�����ͼ��ʾ�ı仯�������������������е�b��
A��������C B��������ˮ���� C���������¶� D��������ѹǿ
��3�����裨2���з�Ӧ�ڵ�2minʱ���������ݻ�ѹ����1L��������ͼ�л��Ƴ��ܷ�ӳH2O��CO���ʵ����仯���Ƶ�ͼ��
��4������CO��O2��K2CO3�ȹ��ɵ������ε��Ϊ���������400mL����ʳ��ˮ�����ϵĵ缫��ӦʽΪCO+CO32--2e-=2CO2������5.6gȼ�ϱ�����ʱ����������Һ��pH=14��������Һ������仯��������������������ģ���
���� ��1������C��H2��CO��ȼ���ȣ���H���ֱ�Ϊ-393.5kJ•mol-1��-285.8kJ•mol-1��-283kJ•mol-1���Լ�ˮ��������Ϊ+44kJ/mol���ɵâ�C��s��+O2��g���TCO2��g������H=-393.5 kJ/mol����H2��g��+$\frac{1}{2}$O2��g���TH2O��l������H=-285.8kJ/mol����CO��g��+$\frac{1}{2}$O2��g��=CO2��g������H=-283.0kJ•mol-1����H2O��g��=H2O��l������H=-44kJ/mol�����ݸ�˹���ɣ�����+��-��-�ۿɵ�̼��ˮ������Ӧ���Ȼ�ѧ����ʽ��
�ڸ����Ȼ�ѧ����ʽ�Լ���Ӧ�зų�����������μӷ�Ӧ��ˮ�������ٸ���ת����=$\frac{��ת�������ʵ���}{��ʼ�����ʵ���}$��100%���㣻
��2���ٸ���ͼ���֪���ڵ�һ��ƽ��ʱ�ε�CO�����ʵ���Ϊ0.2mol�����ʱ���ɵ�H2Ҳ��0.2mol����Ӧ��ϵ��ˮ�����ʵ���Ϊ1.2mol���ɵ�֪���ʵ�ƽ��Ũ�ȣ��ٸ���K=$\frac{c��CO��•c��{H}_{2}��}{c��{H}_{2}O��}$���㣬��Ӧ������2minʱ������ͼ��֪����ͬʱ���ڣ�ˮ��һ����̼�����ʵ����仯������0-1min�ڣ�˵����Ӧ�����������¶ȶԷ�Ӧ���ʡ���ѧƽ����ƶ���Ӱ�������
�ڷ�Ӧ����5minʱ��CO�����ʵ������䣬ˮ�����ʵ�������˵���ı������ˮ�����ʵ�����
��3���������ݻ�ѹ����1L��ѹǿ����Ӧ���ʱ����ƽ�������ƶ���H2O�����ʵ�����ԭ���Ļ����ϻ�����CO���ʵ�����ԭ���Ļ����ϻ��С��
��4����ȼ�ϵ���У�ͨ��CO�ĵ缫Ϊ������������COʧ���Ӻ�̼������ӷ�Ӧ���ɶ�����̼��ˮ��ͨ��O2�ĵ缫Ϊ�����������������õ��ӺͶ�����̼��Ӧ����̼������ӣ����ݵ��ӵ�ʧ�غ������ʳ��ˮ�в��������������ӵ����ʵ���������ȷ��pHֵ���ݴ˴��⣮
��� �⣺��1������C��H2��CO��ȼ���ȣ���H���ֱ�Ϊ-393.5kJ•mol-1��-285.8kJ•mol-1��-283kJ•mol-1���Լ�ˮ��������Ϊ+44kJ/mol���ɵâ�C��s��+O2��g���TCO2��g����H=-393.5 kJ/mol����H2��g��+$\frac{1}{2}$O2��g���TH2O��l����H=-285.8kJ/mol����CO��g��+$\frac{1}{2}$O2��g��=CO2��g����H=-283.0kJ•mol-1����H2O��g��=H2O��l����H=-44kJ/mol�����ݸ�˹���ɣ�����+��-��-�ۿɵ�C��s��+H2O��g��=CO��g��+H2��g����H=+131.3kJ/mol��
�ʴ�Ϊ��C��s��+H2O��g��=CO��g��+H2��g����H=+131.3kJ/mol��
�ڸ����Ȼ�ѧ����ʽC��s��+H2O��g��=CO��g��+H2��g������H=+131.3kJ/mol������������Ϊ191.7kJʱ���μӷ�Ӧ��ˮ���������ʵ���Ϊ$\frac{191.7kJ}{131.3kJ/mol}$=1.46mol������ˮ��ת����=$\frac{1.46}{2}$��100%=73%��
�ʴ�Ϊ��73%��
��2���ٸ���ͼ���֪���ڵ�һ��ƽ��ʱ�ε�CO�����ʵ���Ϊ0.2mol�����ʱ���ɵ�H2Ҳ��0.2mol����Ӧ��ϵ��ˮ�����ʵ���Ϊ1.2mol���ݻ�Ϊ2L�����Դ�ʱCO��ƽ��Ũ��Ϊ0.1mol/L��H2��ƽ��Ũ��Ϊ0.1mol/L��H2O��ƽ��Ũ��Ϊ0.6mol/L����K=$\frac{c��CO��•c��{H}_{2}��}{c��{H}_{2}O��}$=$\frac{0.1��0.1}{0.6}$=0.017��
Ӧ������2minʱ������ͼ��֪����ͬʱ���ڣ�ˮ��һ����̼�����ʵ����仯������0-1min�ڣ�˵����Ӧ��������ˮ���������ʵ������٣�һ����̼�����ʵ������ӣ�˵��ƽ��������Ӧ�����ƶ������÷�ӦΪ���ȷ�Ӧ����øı������ֻ���������¶ȣ�
�ʴ�Ϊ��0.017�����£�
�ڷ�Ӧ����5minʱ��CO�����ʵ������䣬ˮ�����ʵ�������˵���ı����������ˮ�����ʵ������淴Ӧ����ˮ������С��һ����̼����ƽ��������У�
a��������C�ǹ��壬��Ӱ�컯ѧƽ�⣬��a����
b��������ˮ������5minʱ��CO�����ʵ������䣬ˮ�����ʵ�������b��ȷ��
c����Ӧ�����ȷ�Ӧ���������¶�ƽ��������У�ͼ���ϣ���c����
d��������ѹǿ��ƽ��������У�������ͼ��仯����d����
�ʴ�Ϊ��b��
��3���������ݻ�ѹ����1L��ѹǿ����Ӧ���ʱ����ƽ�������ƶ���H2O�����ʵ�����ԭ���Ļ����ϻ�����CO���ʵ�����ԭ���Ļ����ϻ��С������H2O��CO���ʵ����仯���Ƶ�ͼ��Ϊ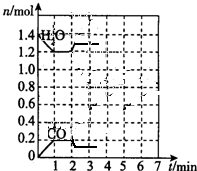 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��4����ȼ�ϵ���У�ͨ��CO�ĵ缫Ϊ������������COʧ���Ӻ�̼������ӷ�Ӧ���ɶ�����̼��ˮ��������ӦʽΪCO+CO32--2e-=2CO2������5.6g����0.2mol��CO������ʱ����·�������ĵ��ӵ����ʵ���Ϊ0.4mol�����ݵ�ⷽ��ʽ2NaCl+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2NaOH+H2��+Cl2����2e-��֪�������в������������Ƶ����ʵ���Ϊ0.4mol�������������Ƶ�Ũ��Ϊ$\frac{0.4}{0.4}$mol/L=1mol/L��������Һ��pH=14��
�ʴ�Ϊ��CO+CO32--2e-=2CO2��14��
���� ���⿼�����Ȼ�ѧ����ʽ��Ӱ�컯ѧ��Ӧ���ʺͻ�ѧƽ���ƶ������ء��缫��Ӧʽ����д�����صļ����֪ʶ�㣬��ȷ��˹���ɺͻ�ѧƽ���ƶ�ԭ�������ӵ�ʧ�غ��ǽ���Ŀ�Ĺؼ�����Ŀ�Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | ������λ��Ԫȡ����ֻ��һ�� | B�� | ���ļ�λ��Ԫȡ����ֻ��һ�� | ||
| C�� | ���Ķ�λ��Ԫȡ����ֻ��һ�� | D�� | ������λ��Ԫȡ�����ж��� |
| ʱ��t��s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO����mol�� | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��2����ͼ1��ʾNO2�仯���ߵ���b��������ĸ����
��3����ʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����c��
a����ʱ�����NO2���� b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч����
e�����µ���ʱ�����뺤�� f�����µ�ѹʱ���뺤��
��4������2mol NO��1mol O2���������ܱ������У�����һ���¶Ƚ��з�Ӧ��2NO��g��+O2��g��?2NO2��g�����ں�ѹ�����´ﵽƽ��ʱ����amol NO2���ں��������´ﵽƽ��ʱ����bmol NO2����a��b�Ĺ�ϵ�ǣ�a��b
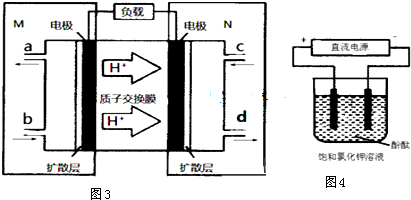
��5��ij��ѧС�鹹�뽫����β����NO��NO2��ת��Ϊ��Ҫ�Ļ���ԭ��HNO3����ԭ������ͼ2��ʾ������A��BΪ��ײ��ϣ�����˵����ȷ����D
A���������Һ�е����ķ�����B��A�����ӵ�������֮�෴
B���õ�ع���ʱ��ÿת��4mol���ӣ�����22.4L O2
C���缫B������c��NO3-������
D���缫A���淴Ӧ֮һΪNO-3e-+2H2O�TNO3-+4H+��
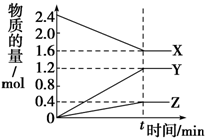 ��2L��������3�����ʽ��з�Ӧ��X��Y��Z�����ʵ�����ʱ��ı仯������ͼ��ʾ����Ӧ��tʱ�̴ﵽƽ�⣮
��2L��������3�����ʽ��з�Ӧ��X��Y��Z�����ʵ�����ʱ��ı仯������ͼ��ʾ����Ӧ��tʱ�̴ﵽƽ�⣮��1���÷�Ӧ�Ļ�ѧ����ʽ��2X?3Y+Z
��2�����ݻ�ѧ��Ӧ2A��g��+5B ��g��?4C��g������д�±��еĿհ�
| A | B | C | |
| ��Ӧ��ʼʱŨ�ȣ�mol/L�� | 4.8 | 0 | |
| 2min���Ũ�ȣ�mol/L�� | 1.2 | 0.8 | |
| 2min�ڵ�Ũ�ȵı仯��mol/L�� | 0.4 | ||
| ��ѧѧ��Ӧ����[mol/��L•min��] | 0.5 |
��ش��������⣺
��1������̿Ҳ�����ڴ�������β���е�NO����1L�����ܱ������м���0.1000molNO��2.030mol�������̿������A��B�������壬�ڲ�ͬ�¶��²��ƽ����ϵ�и����ʵ����ʵ����Լ�������ѹǿ�����
| ����̿/mol | NO/mol | A/mol | B/mol | ��/Mpa | |
| 200�� | 2.000 | 0.0400 | 0.0300 | 0.0300 | 3.93 |
| 335�� | 2.005 | 0.0500 | 0.0250 | 0.0250 | �� |
��2������β���е�SO2����ʯ��ˮ�����գ��������������Һ�������£����ij��CaSO3��ˮ�γɵ���ҺpHΪ9����֪Ka1��H2SO3��=1.8��10-2��Ka2��H2SO3��=6.0��10-9������SO32-�ĵڶ���ˮ�⣬��Ksp��CaSO3��=4.2��10-9��
��3��β���е�̼�⻯���ﺬ�м��飬���������ܵĴ�ת�����пɷ������·�ӦCH4��g��+H2O��1���TCO��g��+3H2 ��g����H=+250.1kJ/mol����֪CO��g����H2 ��g����ȼ��������Ϊ283.0kJ/mol��285.8kJ/mol����д����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽCH4��g��+2O2��g����CO2��g��+2H2O��l����H=-890.3KJ/mol����CH4��g��Ϊȼ�Ͽ�����Ƽ���ȼ�ϵ�أ��õ����ϡH2SO4���������Һ���为���缫��ӦʽΪCH4-8e-+2H2O=CO2+8H+����֪�õ�ص�����ת��Ч��Ϊ86.4%����õ�صı�����Ϊ13.3kW•h•kg-1���������1λС����������=$\frac{���������ܣ�kW•h��}{ȼ��������kg��}$��lkW•h=3.6��106J����
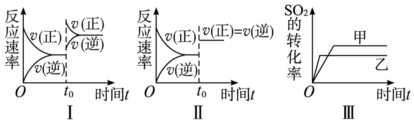
| A�� | ͼ���о�����t0ʱ������O2��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�� | |
| B�� | ͼ���о������¶ȶԻ�ѧƽ���Ӱ�죬���ҵ��¶Ƚϵ� | |
| C�� | ͼ���о����Ǵ�����ƽ���Ӱ�죬�ҼĴ�Ч�ʱ��Ҹ� | |
| D�� | ͼ���о�����t0ʱ�̼��������Է�Ӧ���ʵ�Ӱ�� |
| A�� | $\frac{1}{44}$ mol-1 | B�� | $\frac{x}{22}$ mol-1 | C�� | $\frac{3x}{44}$ mol-1 | D�� | $\frac{44x}{3}$ mol-1 |
 ��һ�������£���������������������·�Ӧ��2SO2��g��+O2��g��?2SO3��g������H��0��
��һ�������£���������������������·�Ӧ��2SO2��g��+O2��g��?2SO3��g������H��0��