题目内容
12. 在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)?2SO3(g)(△H<0)
在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)?2SO3(g)(△H<0)(1)写出该反应的化学平衡常数表达式 K=$\frac{{c{{(S{O_3})}^2}}}{{c(S{O_2})•c({O_2})}}$.
(2)降低温度,该反应K值增大(填增大、减小或不变).
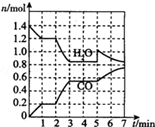
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图所示,反应处于平衡状态的时间有15-20min和25-30min.
(4)据图判断,反应进行至20min时,曲线发生变化的原因是增加了氧气的浓度(或通入氧气)(用文字表达);
(5)10min到15min的曲线变化的原因可能是CD(填写编号).
A.降低温度 B.增加SO3的物质的量
C.加了催化剂 D.缩小容器体积.
分析 (1)K为生成物浓度幂之积与反应物浓度幂之积的比;
(2)该反应为放热反应,降低温度,平衡正向移动;
(3)由图可知,物质的量不变时为平衡状态;
(4)由图可知,反应进行至20min时,氧气的浓度突然增大,平衡正向移动,二氧化硫的浓度减小,三氧化硫的浓度增大;
(5)10min到15min,曲线斜率增大,反应速率加快,以此来解答.
解答 解:(1)由2SO2(g)+O2 (g)?2SO3(g) 可知,K=$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})c({O}_{2})}$,故答案为:$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})c({O}_{2})}$;
(2)该反应为放热反应,降低温度,平衡正向移动,则降低温度,该反应K值增大,故答案为:增大;
(3)由反应过程中SO2、O2、SO3物质的量变化图可知,反应处于平衡状态的时间有15-20min和25-30min,故答案为:15-20min和25-30min;
(4)由图可知,反应进行至20min时,氧气的浓度突然增大,平衡正向移动,二氧化硫的浓度减小,三氧化硫的浓度增大,则曲线发生变化的原因是增加了氧气的浓度(或通入氧气),故答案为:增加了氧气的浓度(或通入氧气);
(5)10min到15min,曲线斜率增大,反应速率加快,加催化剂、缩小容器体积均加快反应速率,降低温度反应速率减小,若增加SO3的物质的量平衡逆向移动,反应物浓度增大与图象不符,故答案为:CD.
点评 本题考查化学平衡的计算,为高频考点,把握K的表达式及影响因素、平衡移动为解答的关键,侧重分析与应用能力的考查,注意图象与平衡移动原理的结合,题目难度不大.

练习册系列答案
相关题目
6.已知:CO(g)+H2O(g)?H2(g)+CO2(g)平衡常数随温度的变化如表:
试回答下列问题
(1)上述化学变化的逆向反应是:吸热 反应(选填:放热、吸热).
(2)800℃发生上述反应,以表中的物质的量投入恒容反应器,
其中向正向移动的有BCE(选填A、B、C、D、E).
(3)已知在一定温度下:C(s)+CO2(g)?2CO(g)△H1平衡常数K;
C(s)+H2O(g)?CO(g)+H2(g)△H2平衡常数K1;
CO(g)+H2O(g)?H2(g)+CO2(g)△H3平衡常数K2,
则K、K1、K2之间的关系是:$\frac{{K}_{1}}{{K}_{2}}$.
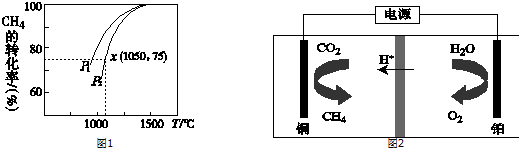
(4)若在500℃时进行,若CO、H2O的起始浓度均为0.020mol/L,在该条件下,CO的最大转化率为:75%.
(5)若800℃进行,设起始时CO和H2O(g)共5mol,水蒸气体积分数为x;平衡时CO转化率为y,则y随x变化的函数关系式为:y=x.(用含x的代数式表达)
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数Kc | 9.94 | 9 | 1 |
(1)上述化学变化的逆向反应是:吸热 反应(选填:放热、吸热).
(2)800℃发生上述反应,以表中的物质的量投入恒容反应器,
| A | B | C | D | E | |
| n(CO2) | 3 | 1 | 0 | 1 | 1 |
| n(H2) | 2 | 1 | 0 | 1 | 2 |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | 1 |
(3)已知在一定温度下:C(s)+CO2(g)?2CO(g)△H1平衡常数K;
C(s)+H2O(g)?CO(g)+H2(g)△H2平衡常数K1;
CO(g)+H2O(g)?H2(g)+CO2(g)△H3平衡常数K2,
则K、K1、K2之间的关系是:$\frac{{K}_{1}}{{K}_{2}}$.
(4)若在500℃时进行,若CO、H2O的起始浓度均为0.020mol/L,在该条件下,CO的最大转化率为:75%.
(5)若800℃进行,设起始时CO和H2O(g)共5mol,水蒸气体积分数为x;平衡时CO转化率为y,则y随x变化的函数关系式为:y=x.(用含x的代数式表达)
7.在Na2S溶液中下列关系不正确( )
| A. | c(Na+)=2c(S2-)+2c(HS-)+2c(H2S) | B. | c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-) | ||
| C. | c(Na+)>c(S2-)>c(OH-)>c(HS-) | D. | c(OH-)=c(H+)+c(HS-)+c(H2S) |
2.下列关于能源的说法不正确的是( )
| A. | 通过煤的气化和液化获得洁净的燃料 | |
| B. | 加快核能、太阳能、沼气等新能源的开发利用 | |
| C. | 减少资源消耗,注重资源的重复使用、资源的循环再生 | |
| D. | 大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源 |


 .
.
 焦炭与CO、H2均是重要的能源,也是重要的化工原料.
焦炭与CO、H2均是重要的能源,也是重要的化工原料.