题目内容
18.证明苯分子中不存在单双键交替的理由是( )| A. | 苯的邻位二元取代物只有一种 | B. | 苯的间位二元取代物只有一种 | ||
| C. | 苯的对位二元取代物只有一种 | D. | 苯的邻位二元取代物有二种 |
分析 苯分子如果是单双键交替结构,则苯的邻位二元取代物有两种,据此解答.
解答 解:无论苯分子中是否存在单双键交替交替结构,其间位二元取代物、对位二元取代物都只有一种,而邻位二元取代物只有一种,所以苯的邻位二元取代物只有一种证明苯分子中不存在单双键交替;
故选:A.
点评 本题考查了有机物的结构与性质,明确苯分子之间的碳碳键是介于单键与双键之间独特的化学键是解题关键,题目难度不大.

练习册系列答案
相关题目
9.下列各组物质中,不能使用分液漏斗进行分离的是( )
| A. | 甲苯和水 | B. | 氯乙烷和水 | C. | 硝基苯和水 | D. | 单质溴和溴苯 |
6.已知:CO(g)+H2O(g)?H2(g)+CO2(g)平衡常数随温度的变化如表:
试回答下列问题
(1)上述化学变化的逆向反应是:吸热 反应(选填:放热、吸热).
(2)800℃发生上述反应,以表中的物质的量投入恒容反应器,
其中向正向移动的有BCE(选填A、B、C、D、E).
(3)已知在一定温度下:C(s)+CO2(g)?2CO(g)△H1平衡常数K;
C(s)+H2O(g)?CO(g)+H2(g)△H2平衡常数K1;
CO(g)+H2O(g)?H2(g)+CO2(g)△H3平衡常数K2,
则K、K1、K2之间的关系是:$\frac{{K}_{1}}{{K}_{2}}$.
(4)若在500℃时进行,若CO、H2O的起始浓度均为0.020mol/L,在该条件下,CO的最大转化率为:75%.
(5)若800℃进行,设起始时CO和H2O(g)共5mol,水蒸气体积分数为x;平衡时CO转化率为y,则y随x变化的函数关系式为:y=x.(用含x的代数式表达)
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数Kc | 9.94 | 9 | 1 |
(1)上述化学变化的逆向反应是:吸热 反应(选填:放热、吸热).
(2)800℃发生上述反应,以表中的物质的量投入恒容反应器,
| A | B | C | D | E | |
| n(CO2) | 3 | 1 | 0 | 1 | 1 |
| n(H2) | 2 | 1 | 0 | 1 | 2 |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | 1 |
(3)已知在一定温度下:C(s)+CO2(g)?2CO(g)△H1平衡常数K;
C(s)+H2O(g)?CO(g)+H2(g)△H2平衡常数K1;
CO(g)+H2O(g)?H2(g)+CO2(g)△H3平衡常数K2,
则K、K1、K2之间的关系是:$\frac{{K}_{1}}{{K}_{2}}$.
(4)若在500℃时进行,若CO、H2O的起始浓度均为0.020mol/L,在该条件下,CO的最大转化率为:75%.
(5)若800℃进行,设起始时CO和H2O(g)共5mol,水蒸气体积分数为x;平衡时CO转化率为y,则y随x变化的函数关系式为:y=x.(用含x的代数式表达)
13.废旧印刷电路板的回收利用可实现资源再生,并减少污染.废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末.
(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是BD(填字母).
A.热裂解形成燃油B.露天焚烧
C.作为有机复合建筑材料的原料D.直接填埋
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64.39kJ•mol-1
2H2O2(l)═2H2O(l)+O2(g)△H=-196.46kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.84kJ•mol-1
在 H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ.mol-1.
(3)控制其他条件相同,印刷电路板的金属粉末用10%H2O2和3.0mol•L-1H2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率(见下表).
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是H2O2分解速率加快.
(4)在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀.制备CuCl的离子方程式是2Cu2++SO32-+2Cl-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl↓+SO42-+2H+..
(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是BD(填字母).
A.热裂解形成燃油B.露天焚烧
C.作为有机复合建筑材料的原料D.直接填埋
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64.39kJ•mol-1
2H2O2(l)═2H2O(l)+O2(g)△H=-196.46kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.84kJ•mol-1
在 H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ.mol-1.
(3)控制其他条件相同,印刷电路板的金属粉末用10%H2O2和3.0mol•L-1H2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率(见下表).
| 温度(℃) | 220 | 330 | 440 | 550 | 660 | 770 | 880 |
| 铜平均溶解速率(×10-3mol•L-1•min-1) | 77.34 | 88.01 | 99.25 | 77.98 | 77.24 | 66.73 | 55.76 |
(4)在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀.制备CuCl的离子方程式是2Cu2++SO32-+2Cl-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl↓+SO42-+2H+..
7.在Na2S溶液中下列关系不正确( )
| A. | c(Na+)=2c(S2-)+2c(HS-)+2c(H2S) | B. | c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-) | ||
| C. | c(Na+)>c(S2-)>c(OH-)>c(HS-) | D. | c(OH-)=c(H+)+c(HS-)+c(H2S) |

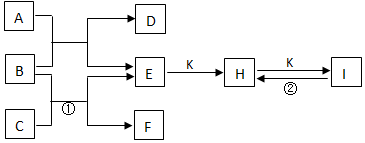
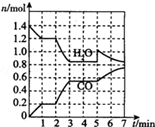 焦炭与CO、H2均是重要的能源,也是重要的化工原料.
焦炭与CO、H2均是重要的能源,也是重要的化工原料.