题目内容
下列说法不正确的是( )
| A、钠是电和热的良导体 |
| B、钠在空气中燃烧生成氧化钠,并发出黄色火焰 |
| C、钠与硫化合时可以发生爆炸 |
| D、钠离子半径比钠原子半径大 |
考点:钠的化学性质
专题:金属概论与碱元素
分析:A.金属都具有良好的导电、导热性;
B.钠在空气中点燃生成的过氧化钠;
C.钠性质非常活泼,在研磨条件下与硫能发生爆炸;
D.依据质子数相同的微粒,电子数越多半径越大.
B.钠在空气中点燃生成的过氧化钠;
C.钠性质非常活泼,在研磨条件下与硫能发生爆炸;
D.依据质子数相同的微粒,电子数越多半径越大.
解答:
解:A.钠属于金属,金属都具有良好的导电、导热性,故A正确;
B.钠在空气中点燃生成的过氧化钠,得不到氧化钠,故B错误;
C.钠性质非常活泼,在研磨条件下与硫能发生爆炸,故C正确;
D.钠离子与钠原子质子数相同,但是钠原子电子数比钠离子多,所以钠原子半径大于钠离子,故D错误;
故选:BD.
B.钠在空气中点燃生成的过氧化钠,得不到氧化钠,故B错误;
C.钠性质非常活泼,在研磨条件下与硫能发生爆炸,故C正确;
D.钠离子与钠原子质子数相同,但是钠原子电子数比钠离子多,所以钠原子半径大于钠离子,故D错误;
故选:BD.
点评:本题考查了元素化合物的性质,熟悉钠的物理性质、化学性质是解题关键,注意微粒半径大小比较的方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
若NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、在25℃,1.01×l05Pa下,1.12L O2含有的分子数是0.05NA |
| B、在25℃,1.01×106Pa下,0.1mol N2含有的原子数是0.2NA |
| C、在同温同压下,同体积任何气体所含原子数相同 |
| D、在同温同压下,两种气体的密度比等于质量之比 |
两种硫酸溶液,一种物质的量浓度为c1,密度为ρ1;另一物质的量浓度为c2,密度为ρ2,将它们等体积混合后,所得溶液的密度为ρ3,则混合后硫酸的物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
在下列物质中,分别加入金属钠,不能产生氢气的是( )
| A、无水酒精 | B、苯 |
| C、蒸馏水 | D、75%的酒精 |
下列说法错误的是( )
| A、下列仪器中①漏斗;②容量瓶;③蒸馏烧瓶;④天平;⑤分液漏斗;⑥滴定管;⑦燃 烧 匙,常用于物质分离的是①③⑤ |
| B、甲酸溶液滴到大理石台板上有气泡产生:2H++CaCO3═CO2↑+Ca2++H2O |
| C、在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉溶解 |
| D、为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量不相等 |
下列分析正确的是( )
| A、将氯气通入H2O2和NaOH的混合溶液中,发出红光,说明反应物的总能量低于生成物的总能量,放出热量 |
| B、1mol H2在氯气中完全燃烧,放出180kJ热量,则键能(E)的关系为E(H-H)=180kJ+2E(H-Cl)-E(Cl-Cl) |
| C、干燥的碘粉与铝粉混合无明显现象,滴上一滴水会冉冉升起紫色的碘蒸气,最后得到白色AlI3.说明碘和铝发生的反应是放热反应 |
| D、精确实验测得H2O在常温下也能微弱电离:H2O?H++OH-,该过程是放热过程 |
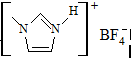 的熔点(填>、=或<),其原因是
的熔点(填>、=或<),其原因是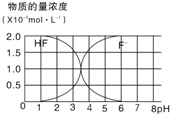 请按要求完成下列各小题:
请按要求完成下列各小题: