题目内容
下列说法错误的是( )
| A、下列仪器中①漏斗;②容量瓶;③蒸馏烧瓶;④天平;⑤分液漏斗;⑥滴定管;⑦燃 烧 匙,常用于物质分离的是①③⑤ |
| B、甲酸溶液滴到大理石台板上有气泡产生:2H++CaCO3═CO2↑+Ca2++H2O |
| C、在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉溶解 |
| D、为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量不相等 |
考点:化学实验方案的评价,铜金属及其重要化合物的主要性质,物质的分离、提纯和除杂,中和滴定
专题:实验评价题
分析:A.①漏斗用于过滤;②容量瓶用于配制溶液;③蒸馏烧瓶用于蒸馏;④天平可称量质量;⑤分液漏斗用于萃取;⑥滴定管用于滴定实验;⑦燃烧匙用于燃烧实验;
B.甲酸为弱酸,在离子反应中保留化学式;
C.Cu为不活泼金属,与稀硫酸不反应,加入Cu(NO3)2固体,具有硝酸的强氧化性可溶解Cu;
D.盐酸易挥发,测定中和热时一般NaOH稍过量.
B.甲酸为弱酸,在离子反应中保留化学式;
C.Cu为不活泼金属,与稀硫酸不反应,加入Cu(NO3)2固体,具有硝酸的强氧化性可溶解Cu;
D.盐酸易挥发,测定中和热时一般NaOH稍过量.
解答:
解:A.①漏斗用于过滤;②容量瓶用于配制溶液;③蒸馏烧瓶用于蒸馏;④天平可称量质量;⑤分液漏斗用于萃取;⑥滴定管用于滴定实验;⑦燃烧匙用于燃烧实验,则过滤、蒸馏、萃取为常见混合物分离方法,即常用于物质分离的是①③⑤,故A正确;
B.甲酸为弱酸,在离子反应中保留化学式,则甲酸溶液滴到大理石台板上有气泡产生的离子反应为2HCOOH+CaCO3═CO2↑+Ca2++H2O+2HCOO-,故B错误;
C.Cu为不活泼金属,与稀硫酸不反应,加入Cu(NO3)2固体,具有硝酸的强氧化性可溶解Cu,发生3Cu+8H++2NO3-=2NO↑+3Cu2++4H2O,故C正确;
D.盐酸易挥发,测定中和热时一般NaOH稍过量,则中和热测定实验中所用酸和碱的物质的量不相等,故D正确;
故选B.
B.甲酸为弱酸,在离子反应中保留化学式,则甲酸溶液滴到大理石台板上有气泡产生的离子反应为2HCOOH+CaCO3═CO2↑+Ca2++H2O+2HCOO-,故B错误;
C.Cu为不活泼金属,与稀硫酸不反应,加入Cu(NO3)2固体,具有硝酸的强氧化性可溶解Cu,发生3Cu+8H++2NO3-=2NO↑+3Cu2++4H2O,故C正确;
D.盐酸易挥发,测定中和热时一般NaOH稍过量,则中和热测定实验中所用酸和碱的物质的量不相等,故D正确;
故选B.
点评:本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、离子反应、氧化还原反应及中和热测定实验等,把握物质的性质及实验原理为解答的关键,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
M元素的一个原子失去两个电子并转移到Y元素的两个原子中,形成离子化合物Z,下列说法不正确的是( )
| A、Z的熔点较高 |
| B、Z可以表示为M2Y |
| C、Z一定溶于水 |
| D、M形成+2价的阳离子 |
下列说法不正确的是( )
| A、钠是电和热的良导体 |
| B、钠在空气中燃烧生成氧化钠,并发出黄色火焰 |
| C、钠与硫化合时可以发生爆炸 |
| D、钠离子半径比钠原子半径大 |
在常温下,下列各物质能使酸性KMnO4溶液褪色又能使溴水褪色并且化学反应原理相同的是( )
| A、SO2 |
| B、CH2═CH2 |
C、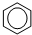 |
| D、CH4 |
下列有关托盘天平的叙述,不正确的是 ( )
| A、称量前先调节托盘天平的零点 |
| B、称量时左盘放被称量物,右盘放砝码 |
| C、潮湿的或具有腐蚀性药品必须放在玻璃器皿中称量,其他固体药品可直接放在天平托盘上称量 |
| D、称量完毕,应把砝码放回砝码盒中 |
| E、用托盘天平可称准到0.01g |
下列不能用勒夏特列原理解释的事实是( )
| A、棕红色的NO2加压后颜色先变深后变浅 |
| B、氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深 |
| C、黄绿色的氯水光照后颜色变浅 |
| D、合成氨工业使用高压以提高氨的产量 |
韩国首尔大学的科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成“暖冰”.下列关于“暖冰”的说法正确的是( )
| A、水凝固形成20℃时的“暖冰”所发生的变化是物理变化 |
| B、“暖冰”中水分子的O-H键是非极性键 |
| C、“暖冰”中存在离子键 |
| D、“暖冰”的密度大,有导电性和导热性 |