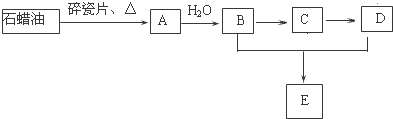
题目内容
两种硫酸溶液,一种物质的量浓度为c1,密度为ρ1;另一物质的量浓度为c2,密度为ρ2,将它们等体积混合后,所得溶液的密度为ρ3,则混合后硫酸的物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:物质的量浓度的相关计算
专题:计算题
分析:令溶液体积都为1L,计算出两种硫酸溶液的质量,混合后的硫酸溶液质量为两种硫酸溶液的质量之和,再利用密度计算混合后的体积,根据混合后硫酸的物质的量为原两种硫酸溶液中硫酸的物质的量计算浓度.
解答:
解:令溶液体积都为1L,则混合后硫酸溶液的质量为1000ml×ρ1g/mL+1000ml×ρ2g/mL=1000(ρ1+ρ2)g.
所以混合后的硫酸溶液的体积为
×10-3L=
L,
令混合后的物质的量浓度为c,则:
1L×c1 mol/L+1L×c2 mol/L═
L×c,
解得c=
,
故选A.
所以混合后的硫酸溶液的体积为
| 1000×(ρ1+ρ2) |
| ρ3 |
| (ρ1+ρ2) |
| ρ3 |
令混合后的物质的量浓度为c,则:
1L×c1 mol/L+1L×c2 mol/L═
| (ρ1+ρ2) |
| ρ3 |
解得c=
| (c1+c2)ρ3 |
| ρ1+ρ2 |
故选A.
点评:本题考查物质的量浓度的计算,为高频考点,把握物质的量浓度、稀释计算公式为解答的关键,侧重分析与计算能力的考查,注意混合溶液体积的计算,题目较简单.

练习册系列答案
相关题目
下列说法正确的是( )
| A、加入过量氨水,有白色沉淀生成,则原溶液一定有Al3+ |
| B、FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体剩余,加入KCSN溶液可能变成血红色 |
| C、常温下铝与浓硫酸不反应,与稀硫酸反应生成氢气 |
| D、加入NaOH溶液,产生气体使湿润的红色石蕊试纸变蓝,则原溶液一定有NH4+ |
中和热的数值是57.3kJ/mol.下列酸、碱溶液混合产生的热量等于57.3kJ的是( )
| A、1mol/L的稀HCl溶液与1mol/L的稀NaOH溶液 |
| B、1mol/L的稀H2SO4溶液与1mol/L的稀Ba(OH)2溶液 |
| C、1L 1mol/L的稀HCl溶液与2L 1mol/L的稀NaOH溶液 |
| D、1L 1mol/L的稀H2SO4溶液与1L 1mol/L的稀Ba(OH)2溶液 |
下列说法不正确的是( )
| A、钠是电和热的良导体 |
| B、钠在空气中燃烧生成氧化钠,并发出黄色火焰 |
| C、钠与硫化合时可以发生爆炸 |
| D、钠离子半径比钠原子半径大 |
在常温下,下列各物质能使酸性KMnO4溶液褪色又能使溴水褪色并且化学反应原理相同的是( )
| A、SO2 |
| B、CH2═CH2 |
C、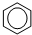 |
| D、CH4 |
下列不能用勒夏特列原理解释的事实是( )
| A、棕红色的NO2加压后颜色先变深后变浅 |
| B、氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深 |
| C、黄绿色的氯水光照后颜色变浅 |
| D、合成氨工业使用高压以提高氨的产量 |