题目内容
9.下列化学用语的表示不正确的是( )| A. | Na2S的电子式: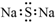 | |
| B. | HClO的结构式:H-O-Cl | |
| C. | 2,2-二甲基丙烷的结构简式: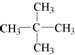 | |
| D. | 氯离子结构示意图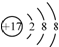 可以表示35Cl-,也可以表示37Cl- 可以表示35Cl-,也可以表示37Cl- |
分析 A.Na2S为离子化合物,钠离子用离子符号表示,硫离子标出最外层电子;
B.氯化氢分子中不存在氢氯键,中心原子为O原子;
C.2,2-二甲基丙烷,主链为丙烷,在2号C含有两个甲基;
D.质子数为17,为氯离子.
解答 解:A.Na2S为离子化合物,钠离子用离子符号表示,硫离子标出最外层电子,硫化钠的电子式为: ,故A错误;
,故A错误;
B.次氯酸分子中含有1个氧氢键和1个氧氯键,次氯酸正确的结构式为:H-O-Cl,故B正确;
C.2,2-二甲基丙烷,主链为丙烷,在2号C含有两个甲基,该有机物结构简式为: ,故C正确;
,故C正确;
D.某离子结构示意图为 ,该离子的质子数为17,则可以表示35Cl-,也可以表示37Cl-,故D正确.
,该离子的质子数为17,则可以表示35Cl-,也可以表示37Cl-,故D正确.
故选A.
点评 本题考查化学用语,涉及电子式、结构式、结构简式以及结构示意图等,注意区别不同的化学用语并规范应用,注重基础知识的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20. 在一定温度和压强条件下发生了反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H<0,反应达到平衡时,改变温度(T)和压强(p),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(p)的关系判断正确的是( )
在一定温度和压强条件下发生了反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H<0,反应达到平衡时,改变温度(T)和压强(p),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(p)的关系判断正确的是( )
 在一定温度和压强条件下发生了反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H<0,反应达到平衡时,改变温度(T)和压强(p),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(p)的关系判断正确的是( )
在一定温度和压强条件下发生了反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H<0,反应达到平衡时,改变温度(T)和压强(p),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(p)的关系判断正确的是( )| A. | P3>P2T3>T2 | B. | P2>P4T4>T2 | C. | P1>P3T3>T1 | D. | P1>P4T2>T3 |
17.铅蓄电池反应如下:Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O,对铅蓄电池工作情况,下列叙述错误的是( )
| A. | 放电时Pb极为负极 | |
| B. | 充电时蓄电池上标有“+”号电极连接电源正极 | |
| C. | 放电时正极反应为PbO2+SO42-+4H++2e═PbSO4+2H2O | |
| D. | 充电时蓄电池上标有“-”号的电极发生氧化反应 |
14.某化工厂采用稀NaOH溶液脱除CO2.若碱洗脱除后所得废液的pH约为13(已知:相同温度下饱和Na2CO3溶液的pH约为12),则下列说法正确的是( )
| A. | 该溶液中:c(OH-)>c(Na+)>c(CO32-)>c(HCO3-)>c(H+) | |
| B. | 该溶液中:c(Na+)+c(H+)═c(OH-)+2c(CO32-)+c(HCO3-) | |
| C. | 加水稀释该溶液,恢复至原温度,pH增大,Kw不变 | |
| D. | 该溶液pH约为13的原因:CO32-+H2O═HCO3-+OH- |
1.对于25℃时的0.1mol.L-1的氨水,下列说法正确的是( )
| A. | 加水稀释后所有的离子浓度均减小 | |
| B. | 与等体积等浓度的盐酸反应后,有:c(NH3.H2O)+c(OH-)=c(H+) | |
| C. | 加入等浓度的盐酸到pH=7时,有:c(NH4+)+c(NH3.H2O)=c(Cl-) | |
| D. | 该溶液在与盐酸完全中和的过程中,H2O的电离度不断增大 |
18.下列说法正确的是( )
| A. | 摩尔是一种物理量 | |
| B. | 溶液中或熔融状态下能导电的物质就是电解质 | |
| C. | 氧化还原反应的本质是元素化合价发生了变化 | |
| D. | 得电子的物质被还原,是氧化剂 |
19.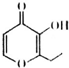 俗称“一滴香”的物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )
俗称“一滴香”的物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )
 俗称“一滴香”的物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )
俗称“一滴香”的物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )| A. | 该有机物的分子式为C8H8O3 | |
| B. | 1 mo1该有机物最多能与 2 mol H2发生加成反应 | |
| C. | 该有机物能发生取代、加成和氧化反应 | |
| D. | 该有机物能与碳酸氢钠反应生成CO2 |
 矿物透闪石是制作玉器的一种原料,其化学式可用CaxMgySi8O22(OH)m表示.
矿物透闪石是制作玉器的一种原料,其化学式可用CaxMgySi8O22(OH)m表示.