题目内容
下列关于阿伏加德罗常数(NA)的说法中正确的是( )
| A、2.4克Mg由原子变为离子,共失去的电子数为0.1NA |
| B、1.7克H2O2中所含有的电子数为0.9NA |
| C、相同质量的NO2和N2O4所含的原子数不同 |
| D、在20℃,1.01×105Pa时,11.2L O2与H2的混合气体所含原子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据1mol镁失去2mol电子来分析;
B、1molH2O2中含18mol电子;
C、根据NO2和N2O4的最简式均为NO2来分析;
D、20℃,1.01×105Pa时,气体摩尔体积大于22.4L/mol.
B、1molH2O2中含18mol电子;
C、根据NO2和N2O4的最简式均为NO2来分析;
D、20℃,1.01×105Pa时,气体摩尔体积大于22.4L/mol.
解答:
解:A、2.4g镁的物质的量为0.1mol,而1mol镁失去2mol电子,故0.1mol镁失去0.2mol电子,故A错误;
B、1.7gH2O2的物质的量为0.05mol,而1molH2O2中含18mol电子,故0.05molH2O2含0.9mol电子,故B正确;
C、NO2和N2O4的最简式均为NO2,故相同质量的NO2和N2O4的气体中含有的NO2的物质的量相同,故含有的原子的物质的量相同,故C错误;
D、20℃,1.01×105Pa时,气体摩尔体积大于22.4L/mol,故11.2L氧气的物质的量小于0.5mol,故原子个数小于NA个,故D错误.
故选B.
B、1.7gH2O2的物质的量为0.05mol,而1molH2O2中含18mol电子,故0.05molH2O2含0.9mol电子,故B正确;
C、NO2和N2O4的最简式均为NO2,故相同质量的NO2和N2O4的气体中含有的NO2的物质的量相同,故含有的原子的物质的量相同,故C错误;
D、20℃,1.01×105Pa时,气体摩尔体积大于22.4L/mol,故11.2L氧气的物质的量小于0.5mol,故原子个数小于NA个,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
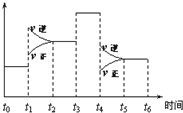 一密闭体系中发生反应:2SO2(g)+O2(g)?2SO3(g),如图表示该反应的速率(v)在某一时间(t)段内的变化.则下列时间段中,SO3的百分含量最高的是( )
一密闭体系中发生反应:2SO2(g)+O2(g)?2SO3(g),如图表示该反应的速率(v)在某一时间(t)段内的变化.则下列时间段中,SO3的百分含量最高的是( )| A、t0→t1 |
| B、t2→t3 |
| C、t3→t4 |
| D、t5→t6 |
下列做法中用到物质氧化性的是( )
| A、铁红做红色颜料 |
| B、水玻璃做木材防火剂 |
| C、氧化铝做耐火材料 |
| D、氯气给自来水杀菌、消毒 |
已知aAn+、bB(n+1)+、cCn-、dD(n+1)-均具有相同的电子层结构,下列判断正确的是( )
| A、元素金属性:B>A;元素非金属性:D>C |
| B、原子半径:A>B>C>D |
| C、离子半径:D(n+1)->C n->B (n+1)+>A n+ |
| D、原子序数:b>a>c>d |
NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A、25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA |
| B、100mL 2 mol/L的NaCl溶液中含NaCl分子数为0.2NA |
| C、常温下,23gNO2和N2O4的混合气体中含有的氮原子数为0.5NA |
| D、标准状况下,22.4L过氧化氢中含有的氧原子数为2NA |
下列说法中正确的是( )
| A、摩尔是表示物质质量的单位 |
| B、10g氟化氢含有0.5molHF分子 |
| C、1g氢气的物质的量是1mol |
| D、物质的摩尔质量等于其式量 |
下列说法正确的是( )
| A、在化学反应中发生物质变化的同时,一定发生能量变化 |
| B、△H>0表示放热反应,△H<0表示吸热反应 |
| C、△H的大小与热化学方程式中化学计量数无关 |
| D、生成物释放的总能量大于反应物吸收的总能量时,△H>0 |
经测定甲醇和环己烷组成混合物中,氧的质量分数为8%,则此混合物中氢的质量分数为( )
| A、78% | B、28% |
| C、14% | D、13% |