题目内容
经测定甲醇和环己烷组成混合物中,氧的质量分数为8%,则此混合物中氢的质量分数为( )
| A、78% | B、28% |
| C、14% | D、13% |
考点:元素质量分数的计算
专题:
分析:CH3OH看作最CH2.H2O,原混合物看作CH2、H2O、C6H12混合,CH2、C6H12的最简式均为CH2,原混合物进一步看作CH2、H2O混合,根据O元素质量分数计算H2O的质量分数,进而计算CH2得到质量分数,再结合化学式CH2计算碳元素质量分数,H元素质量分数=1-w(O)-w(C).
解答:
解:CH3OH看作最CH2.H2O,原混合物看作CH2、H2O、C6H12混合,CH2、C6H12的最简式均为CH2,原混合物进一步看作CH2、H2O混合,氧的质量分数为8%,则H2O的质量分数为8%÷
=9%,故CH2得到质量分数为1-9%=91%,则碳元素质量分数为91%×
=78%,H元素质量分数=1-8%-w78%=14%,故选C.
| 16 |
| 18 |
| 12 |
| 14 |
点评:本题考查质量分数有关计算,难度中等,侧重考查学生分析计算能力,关键是利用物质的化学式改写方法构造出定比组成.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
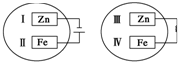 把锌片和铁片放在盛有稀食盐水和K3[Fe(CN)6]试液混合溶液的培养皿中(如图所示平面图),经过一段时间后,下列说法中正确的是( )
把锌片和铁片放在盛有稀食盐水和K3[Fe(CN)6]试液混合溶液的培养皿中(如图所示平面图),经过一段时间后,下列说法中正确的是( )| A、Ⅰ附近溶液pH降低 |
| B、Ⅱ附近很快出现蓝色沉淀 |
| C、Ⅲ附近产生黄绿色气体 |
| D、Ⅳ附近很快生成铁锈 |
下列关于阿伏加德罗常数(NA)的说法中正确的是( )
| A、2.4克Mg由原子变为离子,共失去的电子数为0.1NA |
| B、1.7克H2O2中所含有的电子数为0.9NA |
| C、相同质量的NO2和N2O4所含的原子数不同 |
| D、在20℃,1.01×105Pa时,11.2L O2与H2的混合气体所含原子数为NA |
下列离子方程式正确的是( )
| A、铜片加入稀硝酸中:3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O |
| B、向小苏打溶液中加入醋酸:HCO3-+H+═CO2↑+H2O |
| C、向HI溶液中加入Fe(OH)3固体:Fe(OH)3+3H═Fe3++3H2O |
| D、向MgSO4溶液中加入Ba(OH)2溶液:Ba2++SO42-═BaSO4↓ |
2012年2月新华网报道,加拿大开发出生产医用放射性同位素 9943Tc的简单方法.下列关的叙述正确的是( )
| A、原子序数是99 |
| B、质量数是43 |
| C、中子数是99 |
| D、电子数是43 |
在标准状况下,相同质量的下列气体中体积最大的是( )
| A、Cl2 |
| B、N2 |
| C、CO2 |
| D、H2 |
下列离子方程式书写正确的是( )
| A、金属铁溶于盐酸中:2Fe+6H+=2Fe3++3H2↑ |
| B、氯化铝溶液中加过量氨水:Al3++4OH-=AlO2-+2H2O |
| C、在标准状况下2.24LCO2通入1mol/L 100mLNaOH溶液中:CO2+OH-=HCO3- |
| D、碳酸钡溶于硝酸中:CO32-+2H+=H2O+CO2↑ |
在某一透明溶液中加入Al片有H2生成,则此溶液中一定可大量存在的离子组是( )
| A、AlO2-,K+,SO42-,Cl- |
| B、K+,Br-,SO42-,Na+ |
| C、Fe3+,NO3-,Na+,S2- |
| D、I-,Cl-,Mg2+,SO42- |
下列有关物质存放的说法,正确的是( )
| A、金属钠保存在无水乙醇中 |
| B、冷的浓H2SO4存放于敞口铝制容器中 |
| C、少量的白磷保存在二硫化碳中 |
| D、氯气液化后贮存于钢瓶中 |