题目内容
下列做法中用到物质氧化性的是( )
| A、铁红做红色颜料 |
| B、水玻璃做木材防火剂 |
| C、氧化铝做耐火材料 |
| D、氯气给自来水杀菌、消毒 |
考点:氧化还原反应
专题:
分析:用到物质的氧化性,说明该物质在反应中得电子化合价降低而作氧化剂,据此分析解答.
解答:
解:A.铁红的成分是氧化铁,颜色呈红色,作红色颜料是利用其物理性质,故A错误;
B.水玻璃不燃烧也不支持燃烧,能作木材的防火剂,是利用其物理性质,故B错误;
C.氧化铝熔点很高,一般条件下不熔融,能作耐火材料,是利用其物理性质,故C错误;
D.氯气和水反应生成次氯酸,次氯酸具有强氧化性,能氧化性蛋白质而使其变性,从而杀菌消毒,故D正确;
故选D.
B.水玻璃不燃烧也不支持燃烧,能作木材的防火剂,是利用其物理性质,故B错误;
C.氧化铝熔点很高,一般条件下不熔融,能作耐火材料,是利用其物理性质,故C错误;
D.氯气和水反应生成次氯酸,次氯酸具有强氧化性,能氧化性蛋白质而使其变性,从而杀菌消毒,故D正确;
故选D.
点评:本题考查物质的用途,侧重考查基本性质,明确性质是解本题关键,注意细菌消毒和净水的区别,题目难度不大.

练习册系列答案
 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案
相关题目
2011年为国际化学年,主题为“化学--我们的生活,我们的未来”.下列说法正确的是( )
| A、制作航天服的聚酯纤维和用于光缆通信的晶体硅都是新型无机非金属材料 |
| B、金刚砂的成分是Al2O3,可用作砂纸、砂轮的磨料 |
| C、石油化工广泛使用过渡元素做催化剂并加入少量稀土元素改善催化剂的性能 |
| D、福尔马林(甲醛溶液)可用于浸泡生肉及海产品以防腐保鲜 |
电解质不仅在工农业生产中占有重要地位,而且在各种生命活动中也起着重要作用,则下列有关电解质的叙述正确的是( )
| A、化合物都是电解质 |
| B、电解质一定是化合物 |
| C、SO3溶于水形成的溶液能导电,所以SO3是电解质 |
| D、NaCl固体不导电,所以NaCl不是电解质 |
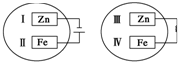 把锌片和铁片放在盛有稀食盐水和K3[Fe(CN)6]试液混合溶液的培养皿中(如图所示平面图),经过一段时间后,下列说法中正确的是( )
把锌片和铁片放在盛有稀食盐水和K3[Fe(CN)6]试液混合溶液的培养皿中(如图所示平面图),经过一段时间后,下列说法中正确的是( )| A、Ⅰ附近溶液pH降低 |
| B、Ⅱ附近很快出现蓝色沉淀 |
| C、Ⅲ附近产生黄绿色气体 |
| D、Ⅳ附近很快生成铁锈 |
某固体化合物M不导电,但熔化或溶于水中能完全电离,下列关于M的说法中,正确的是( )
| A、M为非电解质 |
| B、M是强电解质 |
| C、M为一种盐 |
| D、M是弱电解质 |
在t℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g?mL-1,溶质的质量分数为w,其中含有NH4+的物质的量是b mol,下列叙述正确的是( )
A、溶质的质量分数w=
| ||
B、溶质的物质的量浓度c=
| ||
C、溶液中c(OH-)=
| ||
| D、向上述溶液中加入V mL水,所得溶液的质量分数大于0.5w |
CH3+、-CH3、CH3-都是重要的有机反应中间体,有关它们的说法正确的是( )
| A、它们互为等电子体,碳原子均采取sp2杂化 |
| B、CH3-与NH3、H3O+互为等电子体,中心原子均为sp3杂化,几何构型均为正四面体形 |
| C、CH3+中的碳原子采取sp2杂化,所有原子均共面 |
| D、CH3+与OH-形成的化合物中含有离子键 |
下列关于阿伏加德罗常数(NA)的说法中正确的是( )
| A、2.4克Mg由原子变为离子,共失去的电子数为0.1NA |
| B、1.7克H2O2中所含有的电子数为0.9NA |
| C、相同质量的NO2和N2O4所含的原子数不同 |
| D、在20℃,1.01×105Pa时,11.2L O2与H2的混合气体所含原子数为NA |
下列离子方程式书写正确的是( )
| A、金属铁溶于盐酸中:2Fe+6H+=2Fe3++3H2↑ |
| B、氯化铝溶液中加过量氨水:Al3++4OH-=AlO2-+2H2O |
| C、在标准状况下2.24LCO2通入1mol/L 100mLNaOH溶液中:CO2+OH-=HCO3- |
| D、碳酸钡溶于硝酸中:CO32-+2H+=H2O+CO2↑ |