题目内容
一个原电池反应为:Zn+Cu2+═Zn2++Cu,该原电池的电极及电解质溶液可能是( )
| 正极 | 负极 | 电解质溶液 | |
| A | Zn | Cu | ZnCl2溶液 |
| B | Cu | Zn | 稀H2SO4 |
| C | Cu | Zn | CuSO4溶液 |
| D | 石墨 | Zn | CuSO4溶液 |
| A、A | B、B | C、C | D、D |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电化学专题
分析:根据电池反应式知,失电子的金属作负极,则锌作负极,不如负极活泼的金属或导电的非金属作正极,铜离子得电子发生还原反应,所以电解质溶液中含有铜离子,则电解质溶液为可溶性的铜盐.
解答:
解:锌失电子发生氧化反应而作负极,不如锌活泼的金属或导电的非金属作正极(石墨),铜离子在正极上得电子发生还原反应,则电解质为可溶性的铜盐,符合条件的是C,故选CD.
点评:本题考查了原电池工作原理,判断正负极、电解质溶液时,要根据电池反应式判断:发生氧化反应的电极为负极,发生还原反应的电极为正极,含有发生还原反应的离子溶液为电解质溶液.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
向ZnSO4溶液中加入Na2S溶液时,得到白色沉淀,然后向白色沉淀上滴加CuSO4溶液,发现沉淀变为黑色,则下列说法不正确的是( )
| A、利用该原理可实现一种沉淀转化为更难溶的沉淀 |
| B、该过程破坏了ZnS的溶解平衡 |
| C、白色沉淀为ZnS,而黑色沉淀为CuS |
| D、上述现象说明ZnS的Ksp小于CuS的Ksp |
在一定条件下,在容积为2L的密闭容器中,将2mol 气体M和3mol N气体混合,发生如下反应:2M(g)+3N(g)?x Q(g)+3R(g),该反应达平衡时,生成2.4mol R,并测得Q的浓度为0.4mol/L,下列有关叙述正确的是( )
| A、x值为2 |
| B、混合气体的密度增大 |
| C、平衡时N的浓度为0.3 mol/L |
| D、N的转化率为20% |
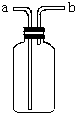 如图所示装置是化学实验中常见的仪器,它除用于洗气外,还有其他用途:
如图所示装置是化学实验中常见的仪器,它除用于洗气外,还有其他用途: 如图是实验室制乙烯的发生装置和乙烯性质实验装置,反应原理为:
如图是实验室制乙烯的发生装置和乙烯性质实验装置,反应原理为: