题目内容
9.下列关于某些离子的检验说法中正确的是( )| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有 CO32- | |
| B. | 某溶液与浓 NaOH 溶液共热,产生使湿润蓝色石蕊试纸变红气体,则原溶液中存在 NH4+ | |
| C. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有 SO 42- | |
| D. | 可用硝酸酸化的 AgNO3 溶液鉴别 Cl-、Br-、I- |
分析 A.无色气体,将气体通入澄清石灰水中,溶液变浑浊,气体为二氧化碳或二氧化硫;
B.氨气使湿润红色石蕊试纸变蓝;
C.白色沉淀为AgCl或硫酸钡;
D.AgNO3 溶液分别与 Cl-、Br-、I-反应的现象为白色沉淀、浅黄色沉淀、黄色沉淀.
解答 解:A.无色气体,将气体通入澄清石灰水中,溶液变浑浊,气体为二氧化碳或二氧化硫,则原溶液可能含CO32-或SO32-,或HCO3-等,故A错误;
B.氨气使湿润红色石蕊试纸变蓝,蓝色石蕊试纸不能检验氨气,故B错误;
C.白色沉淀为AgCl或硫酸钡,则原溶液可能含SO42-或银离子,但二者不能同时存在,故C错误;
D.AgNO3 溶液分别与 Cl-、Br-、I-反应的现象为白色沉淀、浅黄色沉淀、黄色沉淀,现象不同,可鉴别,故D正确;
故选D.
点评 本题考查离子的检验和鉴别,为高频考点,把握离子检验的试剂、现象和结论为解答的关键,侧重分析与实验能力的考查,注意检验时排除干扰离子,题目难度不大.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
相关题目
2.下列叙述不正确的是( )
| A. | 液态HCl不导电,但HCl属于电解质 | |
| B. | NaHSO4溶于水电离出Na+、H+和SO42-,所以NaHSO4属于酸 | |
| C. | 氢氧化铁胶体和食盐水都属于混合物 | |
| D. | Al(OH)3可用作胃酸中和剂,不会对胃壁产生强烈刺激 |
14.C1O2是一种消毒杀菌效率高、二次污染小的水处理剂.我国成功研制出利用NaC102和稀盐酸反应制取C1O2的新方法.关于该反应,下列说法正确的是( )
| A. | 在反应中NaC1O2作氧化剂,稀盐酸作还原剂 | |
| B. | 反应中氧化剂和还原剂的物质的量之比为1:4 | |
| C. | 在反应过程中溶液的酸碱性保持不变 | |
| D. | 在反应中每生成1 mol C1O2转移5 mol电子 |
1.下列指定反应的离子方程式正确的是( )
| A. | 将Na2O2投入足量H2O中:2O22-+2H2O═4OH-+O2↑ | |
| B. | NH4Fe(SO4)2溶液中加入少量NaOH:NH4++OH-═NH3•H2O | |
| C. | 向受酸雨影响的湖泊中撒CaCO3粉末:CO32-+2H+═CO2↑+H2O | |
| D. | 向淀粉-KI溶液中滴加稀硫酸,在空气中一段时间后变蓝:4I-+O2+4H+═2I2+2H2O |
18.室温下,有物质的量浓度相等的下列物质的溶液:①NH4NO3 ②CH3COONH4③NH4HSO4 ④(NH4)2SO4 ⑤(NH4)2CO3,其中所含的c(NH4+)由大到小的顺序是( )
| A. | ②①③⑤④ | B. | ①②③④⑤ | C. | ④⑤③①② | D. | ⑤④③②① |
19.Fe2+与I-都是具有还原性的离子.某研究性学习小组拟用FeI2与氯水反应比较Fe2+与I-的还原性强弱,实验如下:
Ⅰ.实验需要配制250mL0.10mol/LFeI2溶液
(1)配制FeI2溶液除烧杯、量筒、胶头滴管外,还需要的玻璃仪器是玻璃棒、250ml的容量瓶.
(2)如果定容时仰视刻度线,配制的FeI2溶液浓度将偏低(填“偏高”、“偏低”或“无影响”).
Ⅱ.探究Fe2+与I-的还原性强弱
取10mL上述FeI2溶液,向其中滴加少量新制的氯水,振荡后发现溶液呈黄色.同学们对产生黄色的原因提出假设:
假设1:只有I-被少量Cl2氧化成I2溶解在溶液中,还原性:I->Fe2+;
假设2:只有Fe2+被少量Cl2氧化成Fe3+,还原性:Fe2+>I-.
(1)设计方案,验证假设
(2)实验发现假设1正确,写出假设1涉及的离子方程式:2I-+Cl2=2Cl-+I2.
Ⅰ.实验需要配制250mL0.10mol/LFeI2溶液
(1)配制FeI2溶液除烧杯、量筒、胶头滴管外,还需要的玻璃仪器是玻璃棒、250ml的容量瓶.
(2)如果定容时仰视刻度线,配制的FeI2溶液浓度将偏低(填“偏高”、“偏低”或“无影响”).
Ⅱ.探究Fe2+与I-的还原性强弱
取10mL上述FeI2溶液,向其中滴加少量新制的氯水,振荡后发现溶液呈黄色.同学们对产生黄色的原因提出假设:
假设1:只有I-被少量Cl2氧化成I2溶解在溶液中,还原性:I->Fe2+;
假设2:只有Fe2+被少量Cl2氧化成Fe3+,还原性:Fe2+>I-.
(1)设计方案,验证假设
| 实验方案 | 预期现象 | 结论 |
| 向反应后的溶液中加入适量四氯化碳,振荡,静置,分层观察下层液态颜色,在上层溶液中加入KSCN溶液,观察上层颜色 | CCl4层呈紫红色 | 假设1正确 |
| 上层溶液变为红色 | 假设2正确 |
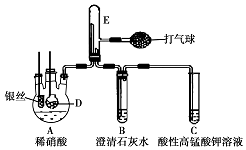 某化学实验小组利用如图装置证明银和稀硝酸反应产生NO,D是内置块状大理石的多孔玻璃笼.(加热装置和夹持装置均已略去.
某化学实验小组利用如图装置证明银和稀硝酸反应产生NO,D是内置块状大理石的多孔玻璃笼.(加热装置和夹持装置均已略去.