题目内容
1.在KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O的反应中,氧化剂是KClO3,还原产物是Cl2,得电子与失电子个数比是1:1,氧化产物与还原产物的质量比是5:1,试用双线桥标出反应电子转移的方向和数目 .
.
分析 由KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O可知,KClO3中Cl元素的化合价由+5价降低为0,HCl中Cl元素的化合价由-1价升高为0,以此来解答.
解答 解:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O的反应中,KClO3中Cl元素的化合价由+5价降低为0,氧化剂是KClO3,被还原,还原产物为Cl2,由电子守恒可知,得电子与失电子个数比是1:1,5个Cl被氧化与1个Cl被还原时转移电子相等,则氧化产物与还原产物的质量比是5:1,该反应转移5e-,双线桥法表示氧化还原反应为 ,
,
故答案为:KClO3;Cl2;1:1;5:1; .
.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案
相关题目
11.下列叙述正确的是( )
| A. | 同温同压下,相同体积的物质,它们的物质的量必相等 | |
| B. | 任何条件下,等质量的氧气和臭氧(O3)所含的原子数必相等 | |
| C. | 1L一氧化碳气体一定比1L氧气的质量小 | |
| D. | 等体积、等物质的量浓度的强酸中所含的H+数一定相等 |
12.下表中列出了25℃、101kPa时一些物质的燃烧热数据
已知键能:C-H键:413.4kJ/mol、H-H键:436.0kJ/mol.则下列叙述正确的是( )
| 物质 | CH4 | C2H2 | H2 |
| 燃烧热/kJ/mol | 890.3 | 1299.6 | 285.8 |
| A. | CH4(g)+2O2(g)═CO2 (g)+2 H2O ( l)△H=-890.3 kJ/mol | |
| B. | 质量相等的CH4比C2H2燃烧放出热量少 | |
| C. | 2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ/mol | |
| D. | 2CH4(g)═C2H2(g)+3H2(g)△H=-376.4 kJ/mol |
9.已知一定温度下,2X(g)+Y(g)?mZ(g)△H=-a kJ/mol(a>0),现有甲、乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器甲中通入2mol X和1mol Y,达到平衡状态时,放出热量b kJ,向密闭容器乙中通入1mol X和0.5mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是( )
| A. | m=4 | B. | a=b | C. | a<$\frac{b}{2}$ | D. | m<3 |
6.A、B均是原子序数为1~18的元素中的一种,已知A的原子序数为n,A2+离子比B2-离子少8个电子,则B的原子序数是( )
| A. | n+4 | B. | n+6 | C. | n+8 | D. | n+10 |
13.下列关于热化学反应的描述中正确的是( )
| A. | 已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则H2SO4和Ba(OH)2反应的反应热△H=2×(-57.3)kJ•mol-1 | |
| B. | 燃料电池中将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9 kJ•mol-1 则CH3OH(g)的燃烧热为192.9 kJ•mol-1 | |
| C. | 葡萄糖的燃烧热是2800 kJ•mol-1,则$\frac{1}{2}$C6H12O6(s)+3O2(g)═3CO2(g)+3H2O(l)△H=-1400 kJ•mol-1 | |
| D. | H2(g)的燃烧热是285.8 kJ•mol-1,则2H2O(g)═2H2(g)+O2(g)△H=+571.6 kJ•mol-1 |
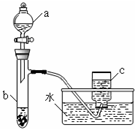 甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答.
甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答.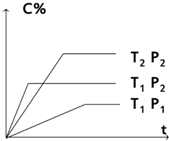 对于反应mA (g)+nB (g)?pC(g) 有如图所示的关系,
对于反应mA (g)+nB (g)?pC(g) 有如图所示的关系,