题目内容
16.历史上金、银、铜主要是作为货币金属或装饰品被应用.(1)金、银、铜常被作为钱币流通,从化学角度来看,主要是利用它们的D.
A.硬度适中
B.密度适中
C.在自然界里都可得到纯净的单质
D.不活泼性
(2)一位收藏者有一枚表面是黑色,且有少量绿色锈状物的货币,这肯定是铜币,黑色物质是氧化铜,形成这种物质的化学方程式为2Cu+O2=2CuO,绿色物质是Cu2(OH)2CO3,形成这种物质的化学方程式为2Cu+O2+CO2+H2O=Cu2(OH)2CO3,这枚金属币的真面目为红色.另外一枚是闪闪发光的黄色金属币,它肯定是金币,表面一直未被氧化的原因是金不活泼,不易被氧化.
(3)不法分子有时用铜锌合金制成假金币行骗.下列方法中能有效鉴别其真假的是D.
A.观察颜色
B.查看图案
C.用手掂量轻重
D.滴一滴硝酸在币的表面,观察现象.
分析 (1)利用金属的不同性质,金属在生产生活中被广泛应用.而用作流通钱币的金、银、铜,根据金属活动性顺序表,金处于表的最后一位,活动性最弱;而银处于倒数第三位,其活动性仅强于金属金和铂;铜处于H元素之后,活动性也较弱;
(2)铜能够与空气中的氧气反应生成黑色的氧化铜,还可以与空气中二氧化碳反应生成绿色的碱式碳酸铜;金化学性质不活泼,不会被空气中氧气氧化;
(3)A.铜锌合金制成的假金元宝,虽然外观上与黄金无异;
B.二者都能做出各种图案;
C.用手掂量轻重误差较大;
D.铜与硝酸反应生成硝酸铜.
解答 解:(1)对比三种金属金、银、铜的活动性可以发现,这三种金属的共性:活动性都比较弱,通常情况下较难与其他物质发生反应.所以金、银、铜常被作为钱币流通,从化学角度来看,主要是利用它们化学性质不活泼的特性,故答案为:D;
(2)铜在铜、银、金中比较活泼,能与空气中氧气发生反应生成氧化铜,2Cu+O2=2CuO,也能与空气中氧气、水及CO2一起发生反应而得到铜锈,所以这些肯定是铜币,绿色物质是碱式碳酸铜,反应的化学方程式为:2Cu+O2+CO2+H2O=Cu2(OH)2CO3;金化学性质稳定,不容易被氧化,闪闪发光的黄色金属币为金币,金不活泼,不易被氧化,故答案为:铜;氧化铜;2Cu+O2=2CuO;Cu2(OH)2CO3;2Cu+O2+CO2+H2O=Cu2(OH)2CO3;红;金;金不活泼,不易被氧化;
(3)A.二者颜色相同,无法鉴别,故A错误;
B.二者都能做出各种图案,无法鉴别,故B错误;
C.金币质量差别较小,用手掂量轻重误差较大,无法鉴别,故C错误;
D.铜与硝酸反应生成硝酸铜,溶液为蓝色,金与硝酸不反应,故D正确.
故选D.
点评 本题考查了常见金属的性质,试题侧重考查了金、银、铜的化学性质,题目难度中等,注意掌握常见金属及其化合物的性质,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

 作业辅导系列答案
作业辅导系列答案| A. | 0.1mol•L-1 | B. | 0.2mol•L-1 | C. | 0.4mol•L-1 | D. | 0.8mol•L-1 |
| A. | 钠浮在水面上,四处游动 | |
| B. | 反应放出的热量使得钠熔化成一个小球 | |
| C. | 反应完后烧杯中有蓝色不溶物 | |
| D. | 反应完后烧杯中出现红色不溶物 |
| A. | 减少对大气的污染 | B. | 降低成本 | ||
| C. | 防止石油短缺 | D. | 加大发动机的动力 |
| A. | 原子序数越大,原子半径一定越大 | |
| B. | 电子层数多的原子的半径一定比电子层数少的大 | |
| C. | 原子序数大的原子,最外层电子数越多 | |
| D. | 元素原子最外层电子数越多(除稀有气体),可显示的化合价不一定越高 |
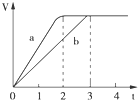 镁粉和铝粉分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )
镁粉和铝粉分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )| A. | 镁粉和铝粉的物质的量之比为3:2 | |
| B. | 镁粉和铝粉质量之比为3:2 | |
| C. | 镁粉和铝粉的摩尔质量之比为2:3 | |
| D. | 镁粉和铝粉反应完所需时间之比为3:2 |
| A. | Na2O2是淡黄色固体,Na2O 是白色固体,二者都能与水反应生成 NaOH | |
| B. | Na和O2在加热时反应生成 Na2O2,在常温下反应生成 Na2O | |
| C. | Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成 O2 | |
| D. | 2 g H2充分燃烧后产物被Na2O2完全吸收,Na2O2固体增重2g |
 .
.