题目内容
12.下列关于电解质溶液的叙述正确的是( )| A. | 常温下,在pH=7的醋酸钠和醋酸混合溶液中:c(CH3COO-)>c(Na+) | |
| B. | 1 mol•L-1的硫化钠溶液中,c(H+)+c(Na+)=c(OH-)+c(HS-)+c(S2-) | |
| C. | 稀释醋酸溶液,溶液中所有离子的浓度均降低 | |
| D. | pH=5的氯化钠和稀硝酸的混合溶液中,c(Na+)=c(Cl-) |
分析 A.溶液中存在电荷守恒分析,溶液呈中性c(H+)=c(OH-);
B.溶液中存在电荷守恒,阴阳离子所带电荷总数相同;
C.醋酸溶液稀释,平衡状态下微粒浓度减小,温度不变离子积常数不变;
D.pH=5的溶液中c(H+)>c(OH-),由电荷守恒可知,c(Na+)+c(H+)=c(OH-)+c(Cl-)+c(NO3-),但钠离子、氯离子均来源氯化钠的电离;
解答 解:A.常温下,在pH=7的醋酸钠和醋酸混合溶液中c(H+)=c(OH-),电荷守恒式为c(H+)+c(Na+)=c(OH-)+c(CH3COO-),则c(CH3COO-)=c(Na+),故A错误;
B.稀释醋酸溶液,c(H+)减小,Kw不变,则醋酸稀释时c(OH-)增大,故B错误;
C.硫化钠溶液中,由电荷守恒可知c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-),由物料守恒可知$\frac{1}{2}$c(Na+)=c(S2-)+c(HS-)+c(H2S),则c(OH-)=c(H+)+c(HS-)+2c(H2S),故C错误;
D.pH=5的溶液中c(H+)>c(OH-),由电荷守恒可知,c(Na+)+c(H+)=c(OH-)+c(Cl-)+c(NO3-),则c(Na+)<c(Cl-)+c(NO3-),但钠离子、氯离子均来源氯化钠的电离,则c(Na+)=c(Cl-),故D正确;
故选D.
点评 本题考查离子浓度大小的比较,明确溶液中电荷守恒、物料守恒、Kw的计算等即可解答,注意选项C为解答的易错点,题目难度不大.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
2.下列各组排列顺序不正确的是( )
| A. | 原子半径:钠>硫>氯 | B. | 氧化性:Na+>K+ | ||
| C. | 最高正化合价:氯>硫>磷 | D. | 酸性:HF>HCl>HBr |
3.下列做法不正确的是( )
| A. | 二氧化硫用作食品防腐剂 | |
| B. | 明矾用于水的净化 | |
| C. | 盛放氢氧化钠溶液时,使用带橡皮塞的磨口瓶 | |
| D. | 在常温下用铝制贮罐贮运浓硫酸 |
7.氨的合成是一项重要的化工生产.已知合成氨有关能量变化的图象如图1.

(1)反应N2(g)+3H2(g)$?_{高温高压}^{催化剂}$2NH3(g)△H=-92KJ/mol;
(2)已知键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.
则表中X的值是391.
(3)在一定条件下按图2实线I进行,改变某条件按图2虚线II进行,则该条件可能是加入催化剂.

(1)反应N2(g)+3H2(g)$?_{高温高压}^{催化剂}$2NH3(g)△H=-92KJ/mol;
(2)已知键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | X | 946 |
(3)在一定条件下按图2实线I进行,改变某条件按图2虚线II进行,则该条件可能是加入催化剂.
4.J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表.J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.
(1)M的离子结构示意图为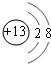 ;元素T在周期表中位于第ⅦA族.
;元素T在周期表中位于第ⅦA族.
(2)J和氢组成10电子的化合物,其分子式为CH4.
(3)M和T的最高价氧化物对应的水化物反应的化学方程式为Al(OH)3+3HClO4═Al(ClO4)3+3H2O.
| J | ||||
| R |
 ;元素T在周期表中位于第ⅦA族.
;元素T在周期表中位于第ⅦA族.(2)J和氢组成10电子的化合物,其分子式为CH4.
(3)M和T的最高价氧化物对应的水化物反应的化学方程式为Al(OH)3+3HClO4═Al(ClO4)3+3H2O.
1.根据表中部分短周期元素的原子半径和主要化合价信息判断,以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.130 | 0.118 | 0.090 | 0.102 | 0.073 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 单质与同浓度稀盐酸反应的速率为L<M | |
| B. | R与T形成的化合物一定能使品红溶液褪色 | |
| C. | 氢化物的稳定性为:H2T>H2R | |
| D. | 当单质L着火时,可用CO2灭火 |
 VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化台物在研究和生产中有许多重要用途.请回答下列问题:
VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化台物在研究和生产中有许多重要用途.请回答下列问题: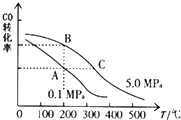 甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题:
甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题: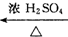 A(C4H8O3)$→_{△}^{浓H_{2}SO_{4}}$乙,甲、乙的分子式都为C4H6O2,甲能使溴的四氯化碳溶液褪色,乙为五元环状化合物,则甲不能发生的反应类型有( )
A(C4H8O3)$→_{△}^{浓H_{2}SO_{4}}$乙,甲、乙的分子式都为C4H6O2,甲能使溴的四氯化碳溶液褪色,乙为五元环状化合物,则甲不能发生的反应类型有( )