题目内容
 硫酸亚铁铵[(NH4)2SO4?FeSO4?6H2O]为浅绿色晶体,易溶于水,不溶于酒精,在水中的溶解度比FeSO4或(NH4)2SO4都要小.实验室中常以废铁屑为原料来制备,其步骤如下:
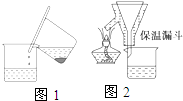
硫酸亚铁铵[(NH4)2SO4?FeSO4?6H2O]为浅绿色晶体,易溶于水,不溶于酒精,在水中的溶解度比FeSO4或(NH4)2SO4都要小.实验室中常以废铁屑为原料来制备,其步骤如下:步骤1:铁屑的处理.将废铁屑放入热的碳酸钠溶液中浸泡几分钟后,用图1所示方法分离出固体并洗涤、干燥.
步骤2:FeSO4溶液的制备.将处理好的铁屑放入锥形瓶,加入过量的3mol?L-1 H2SO4溶液,加热至充分反应为止.趁热过滤(如图2所示),收集滤液和洗涤液.
步骤3:硫酸亚铁铵的制备.向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过加热浓缩、冷却结晶、过滤、乙醇洗涤后得到硫酸亚铁铵晶体.
请回答下列问题:
(1)步骤1中图1分离方法称为
(2)步骤2中有一处明显不合理的是
(3)步骤3加热浓缩过程中,当
考点:制备实验方案的设计
专题:实验设计题
分析:(1)分析装置1是倾析法;
(2)步骤2中加入过量铁粉防止Fe2+被氧化为Fe3+.溶液趁热过滤防止溶液冷却时,硫酸亚铁因析出而损失.
(3)加入(NH4)2SO4固体后,溶液表面出现晶膜时,停止加热,采取蒸发浓缩、冷却结晶方法,通过减压过滤(或抽滤)等得到较为干燥的晶体;
(2)步骤2中加入过量铁粉防止Fe2+被氧化为Fe3+.溶液趁热过滤防止溶液冷却时,硫酸亚铁因析出而损失.
(3)加入(NH4)2SO4固体后,溶液表面出现晶膜时,停止加热,采取蒸发浓缩、冷却结晶方法,通过减压过滤(或抽滤)等得到较为干燥的晶体;
解答:
解:(1)步骤1中图1分离方法称为倾析法;
故答案为:倾析法;
(2)步骤2中加入过量铁粉防止Fe2+被氧化为Fe3+.溶液趁热过滤防止溶液冷却时,硫酸亚铁因析出而损失;
故答案为:应该铁屑过量,否则溶液中可能有Fe3+存在;减少溶质损失;
(3)加入(NH4)2SO4固体后,溶液表面出现晶膜时,停止加热,采取蒸发浓缩、冷却结晶方法,通过减压过滤(或抽滤)等得到较为干燥的晶体,硫酸亚铁铵晶体不溶于乙醇,可以用乙醇洗去晶体表面的水;
故答案为:浓缩至液体表面出现晶膜;硫酸亚铁铵晶体不溶于乙醇,乙醇可以除去其表面的水分;
故答案为:倾析法;
(2)步骤2中加入过量铁粉防止Fe2+被氧化为Fe3+.溶液趁热过滤防止溶液冷却时,硫酸亚铁因析出而损失;
故答案为:应该铁屑过量,否则溶液中可能有Fe3+存在;减少溶质损失;
(3)加入(NH4)2SO4固体后,溶液表面出现晶膜时,停止加热,采取蒸发浓缩、冷却结晶方法,通过减压过滤(或抽滤)等得到较为干燥的晶体,硫酸亚铁铵晶体不溶于乙醇,可以用乙醇洗去晶体表面的水;
故答案为:浓缩至液体表面出现晶膜;硫酸亚铁铵晶体不溶于乙醇,乙醇可以除去其表面的水分;
点评:本题考查了实验步骤的分析判断,物质制备的实验设计方法,性质验证,晶体析出方法的应用,题目难度中等.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
实验室用固态不纯氯化钠(含少量泥沙和Na2SO4杂质)制取纯净氯化钠溶液.下列操作可供选用:①逐滴加入稀盐酸至稍过量;②煮沸;③加蒸馏水溶解;④过滤 ⑤加入稍过量的Na2CO3溶液;⑥加入稍过量的BaCl2溶液.上述实验操作的正确顺序应是( )
| A、①②③④⑤⑥ |
| B、④③⑥⑤①② |
| C、③⑥⑤④①② |
| D、③⑥⑤①④② |
常温下,以MnO2为原料制得的MnCl2溶液中常含有Cu2+、Pb2+、Cd2+等,通过添加过量的难溶电解质MnS,可使这些金属离子形成硫化物沉淀并过滤除去,下列说法正确的是( )
| A、过滤后的溶液中一定没有S2- |
| B、MnS难溶于水,可溶于MnCl2溶液中 |
| C、常温时,CuS、PbS、CdS比MnS更难溶 |
| D、加入MnS后生成CuS的离子方程式是Cu2++S2-=CuS↓ |
关于3Cl2+6KOH
KClO3+5KCl+3H2O反应,以下说法错误的是( )
| ||
| A、Cl2既是氧化剂,又是还原剂 |
| B、3 mol氯气参加反应转移5 mol电子 |
| C、氧化产物的物质的量是还原产物的物质的量的5倍 |
| D、每有1 mol原子被氧化的同时就有5 mol原子被还原 |

 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.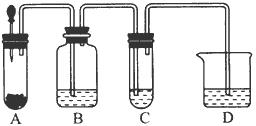 小明在阅读《化学课外补充材料(高一)》时,注意到该书中的下列描述:浓盐酸和次氯酸钙能发生反应并产生氯气,反应为Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.小明设计了如图的装置验证上述反应原理.(已知:胶头滴管中装浓盐酸)
小明在阅读《化学课外补充材料(高一)》时,注意到该书中的下列描述:浓盐酸和次氯酸钙能发生反应并产生氯气,反应为Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.小明设计了如图的装置验证上述反应原理.(已知:胶头滴管中装浓盐酸)