题目内容
0.1mol/L的盐酸和0.1mol/L的氨水等体积混合后,混合后溶液:
(1)呈现 性(选择酸性碱性或中性).
(2)写出粒子浓度大小关系 ;
(3)物料守恒: .
(1)呈现
(2)写出粒子浓度大小关系
(3)物料守恒:
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:(1)室温下,等物质的量浓度、等体积的盐酸和氨水混合,n(HCl)=n(NH3),恰好完全反应生成NH4Cl,为强酸弱碱盐,溶液显酸性,以此来解答;
(2)依据溶液恰好反应生成氯化铵溶液,铵根离子水解分析判断;
(3)抓住氮和氯的物质量相等,而氮的存在形式有两种,得物料守恒.
(2)依据溶液恰好反应生成氯化铵溶液,铵根离子水解分析判断;
(3)抓住氮和氯的物质量相等,而氮的存在形式有两种,得物料守恒.
解答:
(1)0.1mol/L的盐酸和0.1mol/L的氨水等体积混合后,恰好完全反应生成NH4Cl,为强酸弱碱盐,溶液显酸性,故答案为:酸性;
(2)0.1mol/L氨水溶液和0.1mol/L盐酸溶液等体积混合后反应生成氯化铵溶液,铵根离子水解,溶液中离子浓度大小为:c(Cl-)>c(NH4+)>c(H+)>c(OH-),故答案为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);
(3)氮的存在形式有两种分别为:c(NH4+)+c(NH3?H2O)=c(Cl-)=
mol/L=0.05mol/L,故答案为:c(NH4+)+c(NH3?H2O)=c(Cl-)=0.05mol/L.
(2)0.1mol/L氨水溶液和0.1mol/L盐酸溶液等体积混合后反应生成氯化铵溶液,铵根离子水解,溶液中离子浓度大小为:c(Cl-)>c(NH4+)>c(H+)>c(OH-),故答案为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);
(3)氮的存在形式有两种分别为:c(NH4+)+c(NH3?H2O)=c(Cl-)=
| 0.1 |
| 2 |
点评:本题考查酸碱混合及盐类水解,侧重学生分析能力的考查,把握酸碱等物质的量反应恰好生成氯化铵为解答的关键,注重基础知识的夯实,题目难度不大.

练习册系列答案
相关题目
常温时,在pH=13的无色透明溶液中一定能大量共存的一组离子是( )
| A、Na+、SiO32-、NO3-、CO32- |
| B、K+、Cl-、MnO4-、SO42- |
| C、Na+、NO3-、SO42-、HCO3- |
| D、Na+、SO42-、NH4+、Cl- |
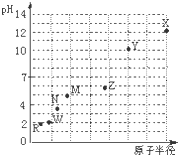 第三周期元素,浓度均为0.01mol/L的最高价氧化物对应水化物的pH与原子半径的关系如图所示.则下列说法正确的是( )
第三周期元素,浓度均为0.01mol/L的最高价氧化物对应水化物的pH与原子半径的关系如图所示.则下列说法正确的是( )| A、气态氢化物的稳定性:M>N |
| B、Z的最高价氧化物对应的水化物能溶于稀氨水 |
| C、X和W形成的常见化合物阴阳离子个数比为1:2 |
| D、Z和R组成的化合物是弱电解质 |
与有机物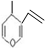 互为同分异构体,且能与NaOH 溶液反应的化合物有( )
互为同分异构体,且能与NaOH 溶液反应的化合物有( )
 互为同分异构体,且能与NaOH 溶液反应的化合物有( )
互为同分异构体,且能与NaOH 溶液反应的化合物有( )| A、7种 | B、8种 | C、9种 | D、10种 |
关于分散系和胶体的说法正确的是( )
| A、胶体、溶液、浊液都是分散系 |
| B、粒子的半径:浊液>溶液>胶体 |
| C、可见光通过溶液时,产生丁达尔现象 |
| D、胶体都不透明,且稳定性极强 |
 对叔丁基杯芳烃的合成原理如下,装置如图:
对叔丁基杯芳烃的合成原理如下,装置如图: +4HCIHO
+4HCIHO +4H2O
+4H2O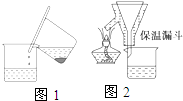 硫酸亚铁铵[(NH4)2SO4?FeSO4?6H2O]为浅绿色晶体,易溶于水,不溶于酒精,在水中的溶解度比FeSO4或(NH4)2SO4都要小.实验室中常以废铁屑为原料来制备,其步骤如下:
硫酸亚铁铵[(NH4)2SO4?FeSO4?6H2O]为浅绿色晶体,易溶于水,不溶于酒精,在水中的溶解度比FeSO4或(NH4)2SO4都要小.实验室中常以废铁屑为原料来制备,其步骤如下:
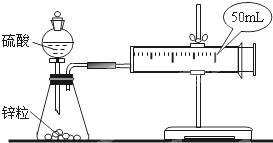 两套如图所示装置,各盛有2g锌粒(颗粒大小相同)分别加入40ml 1mol/L和40ml 4mol/L的硫酸,比较二者收集10ml H2时所用的时间.
两套如图所示装置,各盛有2g锌粒(颗粒大小相同)分别加入40ml 1mol/L和40ml 4mol/L的硫酸,比较二者收集10ml H2时所用的时间.