题目内容
20.工业上用甲苯生产对羟基苯甲酸乙酯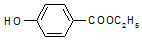 ,生产过程如图:
,生产过程如图: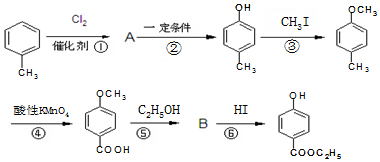
(1)对羟基苯甲酸乙酯的分子式为C9H10O3;1mol 该物质与NaOH溶液完全反应,最多消耗2molNaOH.
(2)化合物A中的官能团名称是氯原子,反应④的反应类型属氧化反应.
(3)反应①的化学方程式
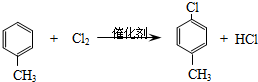 .
.(4)有机物C(分子构型为
 ,-X、-Y为取代基)是对羟基苯甲酸乙酯的同分异构体且能发生银镜反应,则-X的结构简式可能是-OH、-CH2OH 或-OCH3.
,-X、-Y为取代基)是对羟基苯甲酸乙酯的同分异构体且能发生银镜反应,则-X的结构简式可能是-OH、-CH2OH 或-OCH3.
分析 甲苯和氯气发生取代反应生成A,A发生水解反应生成对甲基苯酚,根据对甲基苯酚结构简式知,甲苯中甲基对位上的氢原子苯氯原子取代,则A结构简式为 ;对甲基苯酚和碘烷发生取代反应生成对甲基苯甲醚,对甲基苯甲醚被酸性高锰酸钾溶液氧化生成对羧基苯甲醚,对羧基苯甲醚和乙醇发生酯化反应生成B,B结构简式为
;对甲基苯酚和碘烷发生取代反应生成对甲基苯甲醚,对甲基苯甲醚被酸性高锰酸钾溶液氧化生成对羧基苯甲醚,对羧基苯甲醚和乙醇发生酯化反应生成B,B结构简式为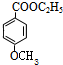 ,B发生取代反应生成对羟基苯甲酸乙酯,结合题目分析解答.
,B发生取代反应生成对羟基苯甲酸乙酯,结合题目分析解答.
解答 解:甲苯和氯气发生取代反应生成A,A发生水解反应生成对甲基苯酚,根据对甲基苯酚结构简式知,甲苯中甲基对位上的氢原子苯氯原子取代,则A结构简式为 ;对甲基苯酚和碘烷发生取代反应生成对甲基苯甲醚,对甲基苯甲醚被酸性高锰酸钾溶液氧化生成对羧基苯甲醚,对羧基苯甲醚和乙醇发生酯化反应生成B,B结构简式为
;对甲基苯酚和碘烷发生取代反应生成对甲基苯甲醚,对甲基苯甲醚被酸性高锰酸钾溶液氧化生成对羧基苯甲醚,对羧基苯甲醚和乙醇发生酯化反应生成B,B结构简式为 ,B发生取代反应生成对羟基苯甲酸乙酯,
,B发生取代反应生成对羟基苯甲酸乙酯,
(1)对羟基苯甲酸乙酯的结构简式为
故答案为,C9H10O3;2;
(2)A结构简式为 ,A中官能团是氯原子,反应④为氧化反应,
,A中官能团是氯原子,反应④为氧化反应,
故答案为:氯原子;氧化反应;
(3)反应①是甲苯与氯气在催化剂条件下发生甲基对位取代生成 ,同时还生成HCl,反应方程式为
,同时还生成HCl,反应方程式为 ,
,
故答案为: ;
;
(4)有机物C(分子构型为 ,-X、-Y为取代基)是对羟基苯甲酸乙酯的同分异构体且能发生银镜反应,含有醛基,X为-OH时,Y为-CH2CH2CHO或-CH(CH3)CHO,X为-CH2OH或-OCH3时,Y为-CHO,即X为-OH、-CH2OH 或-OCH3,故答案为:-OH;-CH2OH 或-OCH3.
,-X、-Y为取代基)是对羟基苯甲酸乙酯的同分异构体且能发生银镜反应,含有醛基,X为-OH时,Y为-CH2CH2CHO或-CH(CH3)CHO,X为-CH2OH或-OCH3时,Y为-CHO,即X为-OH、-CH2OH 或-OCH3,故答案为:-OH;-CH2OH 或-OCH3.
点评 本题考查有机物推断、官能团性质、有机反应类型、同分异构体等,注重学生对知识的强化训练,较好地考查学生对知识的迁移运用、分析推理等能力,明确官能团及其性质、物质之间的转化是解本题关键,题目难度中等.

 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
已知:K300°C>K350°C,则该反应是放热反应.
(2)图中表示NO2的变化的曲线是b.用O2表示从0~2s内该反应的平均速率v=1.5×10-3mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是bc.
a.v (NO2)=2v (O2) b.容器内压强保持不变
c.v逆(NO)=2v正 (O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是c.
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
HNO2是一种弱酸,部分弱酸的电离平衡常数如下表:
| 弱酸 | HNO2 | HClO | H2CO3 | H2SO3 |
| 电离平衡常数 (25℃) | Ki=5.1×10-4 | Ki=2.98×10-8 | $\begin{array}{l}{K_{i1}}=4.3×{10^{-7}}\\{K_{i2}}=5.6×{10^{-11}}\end{array}$ | $\begin{array}{l}{K_{i1}}=1.54×{10^{-2}}\\{K_{i2}}=1.02×{10^{-7}}\end{array}$ |
(6)下列离子方程式正确的是BD
A.2ClO-+H2O+CO2→2HClO+CO32-
B.2HNO2+CO32-→2NO2-+H2O+CO2↑
C.H2SO3+CO32-→CO2+H2O+SO32-
D.Cl2+H2O+2CO32-→2HCO3-+Cl-+ClO-
(7)常温下,pH=3的HNO2溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为c(NO2-)>c(Na+)>c(H+)>c(OH-).
| A. | C3H6与C5H10 | B. | 邻二甲苯与对二甲苯 | ||
| C. | C2H6与C5H12 | D. | 溴乙烷与1,2-二溴乙烷 |
| A. | 进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须大于水 | |
| B. | H2还原CuO时,先通H2后加热CuO,反应完毕后,先停止通H2后撤酒精灯 | |
| C. | 进行蒸馏操作时,冷凝管中的冷凝水应从下口进,上口出 | |
| D. | 当夜晚室内煤气泄漏时,先打开灯,再迅速开窗通气 |
 Ⅰ.某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
Ⅰ.某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步: