题目内容
7.在有机合成中,常利用反应:R-CN+2H2O+H+-→R-COOH+NH4+引入羧基,而-CN可以通过CO与HCN反应引入:过
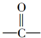 与HCN反应引入:
与HCN反应引入: $→_{一定条件}^{HCN}$
$→_{一定条件}^{HCN}$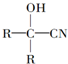
现有某有机物的合成途径为:
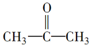 $→_{一定条件①}^{HCN}$A$\underset{\stackrel{{H}_{2}O,{H}^{+}}{→}}{②}$B$→_{③}^{浓H_{2}SO_{4},△}$C$→_{催化剂④}^{聚合}$D
$→_{一定条件①}^{HCN}$A$\underset{\stackrel{{H}_{2}O,{H}^{+}}{→}}{②}$B$→_{③}^{浓H_{2}SO_{4},△}$C$→_{催化剂④}^{聚合}$D(1)写出A、D的结构简式:A
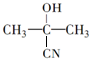 ,D
,D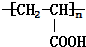 .
.(2)有机物B中含有的官能团名称为羧基和羟基.
(3)下列反应类型为:①加成反应,③消去反应.
(4)写出B→C的化学方程式
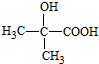 $→_{△}^{浓硫酸}$CH2=CHCOOH+H2O.
$→_{△}^{浓硫酸}$CH2=CHCOOH+H2O.写出两分子B反应生成的环状酯的结构简式
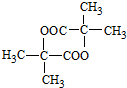 .
.
分析 丙酮与HCN发生加成反应生成A为 ,A水解生成B为
,A水解生成B为 ,B发生消去反应生成C为CH2=CHCOOH,C发生加聚反应生成D为
,B发生消去反应生成C为CH2=CHCOOH,C发生加聚反应生成D为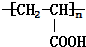 .
.
解答 解:丙酮与HCN发生加成反应生成A为 ,A水解生成B为
,A水解生成B为 ,B发生消去反应生成C为CH2=CHCOOH,C发生加聚反应生成D为
,B发生消去反应生成C为CH2=CHCOOH,C发生加聚反应生成D为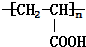 .
.
(1)A的结构简式为,D的结构简式为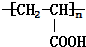 ,故答案为:
,故答案为: ;
;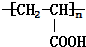 ;
;
(2)有机物B为 ,含有的官能团名称为羧基、羟基,故答案为:羧基、羟基;
,含有的官能团名称为羧基、羟基,故答案为:羧基、羟基;
(3)反应①属于加成反应,反应③属于消去反应,故答案为:加成反应;消去反应;
(4)B→C的化学方程式: $→_{△}^{浓硫酸}$CH2=CHCOOH+H2O,两分子B反应生成的环状酯的结构简式为:
$→_{△}^{浓硫酸}$CH2=CHCOOH+H2O,两分子B反应生成的环状酯的结构简式为: ,
,
故答案为: $→_{△}^{浓硫酸}$CH2=CHCOOH+H2O;
$→_{△}^{浓硫酸}$CH2=CHCOOH+H2O; .
.
点评 本题考查有机物的推断与合成,根据反应条件进行推断,较好的考查学生信息获取与迁移运用,熟练掌握官能团的性质与转化.

练习册系列答案
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
16.用0.1mol•L-1 NaOH溶液分别滴定体积均为20mL浓度均为0.1mol•L-1 HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化曲线如图所示,下列有关说法中正确的是( )

| A. | HX为弱酸,且电离平衡常数Ka≈1×10-10 | |
| B. | 水的电离程度:M点大于N点 | |
| C. | P点c(Cl-)=0.05mol•L-1. | |
| D. | M点c(HX)-c(X-)>c(OH-)-c(H+) |
15.下列各组元素中,非金属性依次增大的是( )
| A. | I、Br、Cl | B. | Al、P、Si | C. | O、S、Na | D. | N、C、B |
12.我国稀土资源丰富.下列有关稀土元素${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm的说法正确的是( )
| A. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm互为同位素 | |
| B. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm的质量数相同 | |
| C. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm是同一种核素 | |
| D. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm是不同元素 |
16.铅蓄电池在现代生活中具有广泛的应用.已知铅蓄电池的电解质溶液为H2SO4溶液,其充电、放电按下式进行2PbSO4+2H2O$?_{放电}^{充电}$Pb+PbO2+2H2SO4,有关该电池的说法正确的是( )
| A. | 放电时溶液中的H+向负极移动 | |
| B. | 在放电时,正极发生的反应是 Pb(s)+SO42-(aq)=PbSO4(s)+2e- | |
| C. | 在放电时,该电池的负极材料是铅板 | |
| D. | 放电时负极反应:PbSO4+2H2O-2e-=PbO2+4H++SO42- |

 .
.