题目内容
17.A、B、C、D、E是位于短周期的主族元素.已知:①热稳定性:HmD>HmC;
②Cm-、E(m-1)-具有相同的电子层结构;
③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;
④A与B质子数之和是D质子数的3倍.
依据上述信息用相应的化学用语回答下列问题:
(1)HmDm的电子式
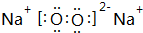 .
.(2)Cm-、E(m-1)-的还原性强弱顺序为:S2->Cl-,(用离子符号表示)能证明其还原性强弱的离子方程式为Cl2+S2-=2Cl-+S↓.
(3)写出B单质与A元素的最高价氧化物对应水化物的溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
分析 A、B、C、D、E是位于短周期的主族元素.
①热稳定性:HmD>HmC,则非金属性D大于C且二者位于同一主族,所以D位于第二周期、C位于第三周期;
②Cm-、E(m-1)- 具有相同的电子层结构,则E的原子序数比C大1,二者位于同一周期,都属于第三周期;
③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小,且二者都为主族元素,则A位于第IA族、B位于第IIIA主族;
④A与B质子数之和是D质子数的3倍,D为第二周期元素,则A和B的质子数之和在9到27之间,A位于第IA族、B位于第IIIA主族,如果A是Li、B是B元素,二者质子数之和不是3的倍数,所以A是Na、B是Al元素,D是O元素,D和C位于同一主族,则C是S元素,E是Cl元素,且m=2.
解答 解:A、B、C、D、E是位于短周期的主族元素.
①热稳定性:HmD>HmC,则非金属性D大于C且二者位于同一主族,所以D位于第二周期、C位于第三周期;
②Cm-、E(m-1)- 具有相同的电子层结构,则E的原子序数比C大1,二者位于同一周期,都属于第三周期;
③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小,且二者都为主族元素,则A位于第IA族、B位于第IIIA主族;
④A与B质子数之和是D质子数的3倍,D为第二周期元素,则A和B的质子数之和在9到27之间,A位于第IA族、B位于第IIIA主族,如果A是Li、B是B元素,二者质子数之和不是3的倍数,所以A是Na、B是Al元素,D是O元素,D和C位于同一主族,则C是S元素,E是Cl元素,且m=2.
(1)A是Na、D是O元素,则HmDm是Na2O2,电子式为 ,故答案为:
,故答案为: ;
;
(2)元素的非金属性越强,其简单阴离子的还原性越弱,S元素的非金属性小于Cl元素,所以Cm-、E(m-1)-的还原性强弱顺序为S2->Cl-,氯气能氧化硫离子生成硫单质,能证明其还原性强弱,反应方程式为Cl2+S2-=2Cl-+S↓,
故答案为:S2->Cl-;Cl2+S2-=2Cl-+S↓;
(3)Al与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评 本题考查位置结构性质的关系及应用,正确推断元素是解本题关键,侧重考查学生分析推理能力、元素周期律及元素化合物性质.

| A. | 短周期主族元素原子的最外层电子数都等于元素的最高化合价 | |
| B. | 多电子原子中,在离核较近的区域内运动的电子能量较高 | |
| C. | 同周期第ⅡA族与第ⅢA族的元素原子序数之差不一定为1 | |
| D. | 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
| 周期 期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)画出原子的结构示意图:⑤
 ;⑪
;⑪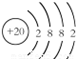 .
.(3)在①~⑫元素中,金属性最强的元素是K,非金属性最强的元素是F,最不活泼的元素是Ar.(均填元素符号)
(4)元素⑦与元素⑧相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b.
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素跟它同周期中原子半径最小的元素(稀有气体除外)可以形成离子(填离子或共价)化合物.
(6)元素⑥是构成地壳的主要元素之一,其氧化物是现代光学及光纤制品的基本原料,该氧化物的化学式为SiO2该氧化物中含有的化学键是共价键(填“离子”或“共价”)
(7)元素①是动植物生长不可缺少的元素,是蛋白质的重要成分.其氢化物常用作制冷剂,该氢化物的电子式为:
 ;在一定条件下,若将元素①的单质和氢气的混合气体通入4L的密闭容器中发生反应,半分钟后测得生成物的物质的量为1.4mol,则用元素①的单质表示的反应速率为0.35mol/(L.min).
;在一定条件下,若将元素①的单质和氢气的混合气体通入4L的密闭容器中发生反应,半分钟后测得生成物的物质的量为1.4mol,则用元素①的单质表示的反应速率为0.35mol/(L.min). ①CuS不溶于醋酸溶液;
②CuS不溶于浓盐酸;
③CuS不溶于浓硫酸;
④CuS在浓硝酸中溶解,溶液变蓝,并有红棕色刺激性气体产生.
根据上述现象,该同学得出了以下结论,其中正确的是( )
| A. | CuS不溶于弱酸,能溶于强酸 | |
| B. | CuS不溶于非氧化性酸,能溶于氧化性酸 | |
| C. | CuS溶于硝酸,是因为硝酸氧化性强于硫酸,S2-被氧化,使CuS溶解 | |
| D. | CuS溶于硝酸,是因为硝酸的酸性大于硫酸和盐酸的酸性,S2-结合H+,放出H2S气体,使CuS溶解 |
| A. | 加入催化剂,改变了反应的途径,反应放出的热量也一定发生变化 | |
| B. | 改变压强,平衡不发生移动,反应放出的热量不变 | |
| C. | 升高温度,反应速率加快,反应放出的热量不变 | |
| D. | 若在原电池中进行,反应放出的热量不变 |
| A. | 必然引起物质状态的变化 | B. | 会产生新的物质 | ||
| C. | 必然会引起化学键的变化 | D. | 必然伴随着能量的变化 |
| A. | 石油主要是各种烷烃、环烷烃组成的混合物 | |
| B. | 做衣服的棉和麻均与淀粉互为同分异构体 | |
| C. | 蔗糖和麦芽糖二者互为同分异构体,且都是还原性糖 | |
| D. | 苯、油脂均能使酸性KMnO4溶液褪色 |
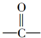 与HCN反应引入:
与HCN反应引入: $→_{一定条件}^{HCN}$
$→_{一定条件}^{HCN}$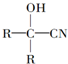
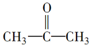 $→_{一定条件①}^{HCN}$A$\underset{\stackrel{{H}_{2}O,{H}^{+}}{→}}{②}$B$→_{③}^{浓H_{2}SO_{4},△}$C$→_{催化剂④}^{聚合}$D
$→_{一定条件①}^{HCN}$A$\underset{\stackrel{{H}_{2}O,{H}^{+}}{→}}{②}$B$→_{③}^{浓H_{2}SO_{4},△}$C$→_{催化剂④}^{聚合}$D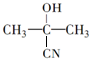 ,D
,D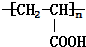 .
.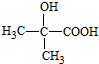 $→_{△}^{浓硫酸}$CH2=CHCOOH+H2O.
$→_{△}^{浓硫酸}$CH2=CHCOOH+H2O.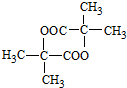 .
.