题目内容
4.工业上,可用如图所示装置来制取KIO3,则下列有关说法错误的是( )
| A. | 图中膜为阴膜(只允许阴离子通过),OH-从右往左通过该膜 | |
| B. | 电解时,阴极电极反应式为:2H++2e-═H2↑ | |
| C. | 电解时,如有3mol电子通过导线,则一定生成0.6mol KIO3 | |
| D. | 电池总反应为:KI+3H2O $\frac{\underline{\;电解\;}}{\;}$KIO3+3H2↑ |
分析 用如图所示装置来制取KIO3,阳极发生氧化反应生成KIO3,电极反应为:I--6e-+3H2O=IO3-+6H+,阴极发生还原反应生成氢气,电极方程式为2H++2e-═H2↑,总方程式为KI+3H2O $\frac{\underline{\;电解\;}}{\;}$KIO3+3H2↑,以此解答该题.
解答 解:A.电解时阴离子向阳极移动,则OH-从右往左通过该膜,故A正确;
B.阴极发生还原反应生成氢气,电极方程式为2H++2e-═H2↑,故B正确;
C.电极反应为:I--6e-+3H2O=IO3-+6H+,如有3mol电子通过导线,则一定生成0.5mol KIO3,故C错误;
D.阳极生成KIO3,阴极生成氢气,总方程式为KI+3H2O $\frac{\underline{\;电解\;}}{\;}$KIO3+3H2↑,故D正确.
故选C.
点评 本题考查了电解原理,为高频考点,侧重学生的分析能力的考查,注意从化合价的角度判断电极反应,根据电池反应式判断阴阳极材料、电极反应,并结合盐的性质分析解答,难度中等.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
14.下列各组溶液中,能用酸式滴定管取用的是( )
| A. | HF | B. | NaHCO3 | C. | HCl | D. | NaHSO3 |
15.化学与生产、生活密切相关,下列说法错误的是( )
| A. | 硅胶有吸水性,是常用的食品干燥剂 | |
| B. | 铝制餐具不能长时间存放酸性、碱性或咸的食物 | |
| C. | 瓷器中含有大量的金属元素,因此陶瓷属于金属材料 | |
| D. | NaCl可以用作调味品和食品防腐剂 |
19.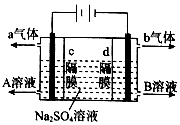 利用三室式电解池(装置结构如图所示,电极均为惰性电极)可以实现用硫酸钠溶液制取硫酸和氢氧化钠.下列叙述正确的是( )
利用三室式电解池(装置结构如图所示,电极均为惰性电极)可以实现用硫酸钠溶液制取硫酸和氢氧化钠.下列叙述正确的是( )
 利用三室式电解池(装置结构如图所示,电极均为惰性电极)可以实现用硫酸钠溶液制取硫酸和氢氧化钠.下列叙述正确的是( )
利用三室式电解池(装置结构如图所示,电极均为惰性电极)可以实现用硫酸钠溶液制取硫酸和氢氧化钠.下列叙述正确的是( )| A. | a气体为氢气,b气体为氧气 | |
| B. | A为氢氧化钠溶液,B为硫酸溶液 | |
| C. | 通电后中间隔室的SO42-向阴极移动,阳极区溶液的pH增大 | |
| D. | 该电解反应的方程式为2Na2SO4+6H2O$\frac{\underline{\;电解\;}}{\;}$2H2SO4+4NaOH+O2↑+2H2↑ |
9.用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 L乙烯含有的共用电子对数为5NA | |
| B. | 8.0gCu2S和CuO的混合物中含有的铜原子数为0.1NA | |
| C. | 电解饱和食盐水时,阳极生成22.4L气体时,转移的电子数为2NA | |
| D. | 室温下向1L pH=1的醋酸溶液中加水,所得溶液中H+数目小于0.1NA |
16.下列物质属于非电解质的是( )
| A. | 液氯 | B. | 酒精 | C. | 氯化钠 | D. | 水 |
1.用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.05mol Cu2(OH)2CO3后恰好恢复到电解前的浓度和pH.则电解过程中转移的电子为( )
| A. | 0.1 mol | B. | 0.2 mol | C. | 0.3 mol | D. | 0.4 mol |
 (R为烃基),其中一种辣椒素酯类化合物J的合成路线如图:
(R为烃基),其中一种辣椒素酯类化合物J的合成路线如图: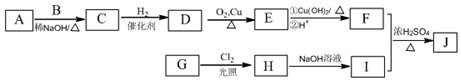
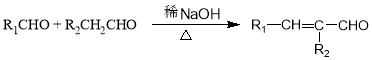
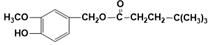 .
.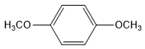 (写结构简式).
(写结构简式).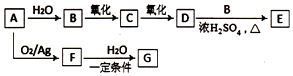 A是一种重要的化工原料,C、F的分子式都为C2H4O,F是没有不饱和键的环状有机物,G的分子式为C2H6O2,G中含有两个相同的官能团,转化关系如图:
A是一种重要的化工原料,C、F的分子式都为C2H4O,F是没有不饱和键的环状有机物,G的分子式为C2H6O2,G中含有两个相同的官能团,转化关系如图: .
.