题目内容
16.下列物质属于非电解质的是( )| A. | 液氯 | B. | 酒精 | C. | 氯化钠 | D. | 水 |
分析 在水溶液或熔融状态下能够导电的化合物为电解质,在水溶液和熔融状态下都不能导电的化合物为非电解质,无论电解质还是非电解质,都一定为化合物,据此进行判断.
解答 解:A.液氯是单质,既不是电解质也不是非电解质,故A错误;
B.酒精溶于水不发生电离,溶液不导电,是非电解质,故B正确;
C.氯化钠在水溶液或熔融状态下能够电离出离子,是电解质,故C错误;
D.水可以电离出氢离子和氢氧根离子,是电解质,故D错误;
故选B.
点评 本题考查了电解质与非电解质的判断,题目难度不大,注意明确电解质与非电解质、强电解质与弱电解质的概念,特别注意:不是电解质的物质不一定属于非电解质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.下列实验设计及其对应的离子方程式均正确的是( )
| A. | 把铁片插入CuSO4溶液中,验证古代湿法冶铜:2Fe+3Cu2+═2Fe3++3Cu | |
| B. | 某气体使澄清石灰水先变浑浊后变澄清,验证该气体是CO2:Ca2++2OH-+CO2═CaCO3↓+H2O、CaCO3+CO2+H2O═Ca2++2HCO3- | |
| C. | 在小苏打溶液中加入醋酸,验证醋酸比碳酸的酸性强:HCO3-+H+═CO2↑+H2O | |
| D. | 若要求用两种单质和一种溶液来测定Zn、Cu、Ag三种金属的活动性顺序,可用Zn、Cu和AgNO3:Zn+2Ag+═Zn2++2Ag |
7.氯的原子序数为17,35Cl是氯的一种同位素,下列说法正确的是( )
| A. | 35Cl原子所含质子数为18 | |
| B. | $\frac{1}{18}$mol的1H35Cl的分子所含中子数约为6.02×1023 | |
| C. | 3.5Cl2气体的体积约为22.4L | |
| D. | 35Cl2气体的摩尔质量为70 |
4.工业上,可用如图所示装置来制取KIO3,则下列有关说法错误的是( )


| A. | 图中膜为阴膜(只允许阴离子通过),OH-从右往左通过该膜 | |
| B. | 电解时,阴极电极反应式为:2H++2e-═H2↑ | |
| C. | 电解时,如有3mol电子通过导线,则一定生成0.6mol KIO3 | |
| D. | 电池总反应为:KI+3H2O $\frac{\underline{\;电解\;}}{\;}$KIO3+3H2↑ |
11.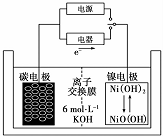 一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )
一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )
 一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )
一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )| A. | 充电时阴极发生氧化反应 | |
| B. | 充电时将碳电极与电源的正极相连 | |
| C. | 放电时碳电极反应为原电池的负极 | |
| D. | 放电时镍电极反应为Ni(OH)2-e-+OH-=NiO(OH)+H2O |
1.下列说法不正确的是( )
| A. | 二氧化硫和氯气都能使品红溶液褪色 | |
| B. | 漂白粉暴露在空气中久置会变质 | |
| C. | 在加热条件下,镁能在二氧化碳气体中燃烧 | |
| D. | 氯水中真正起漂白、杀菌、消毒作用的微粒是其中含有的Cl2分子 |
8.下列说法正确的是( )
| A. | 油脂属于天然高分子化合物,在碱性条件下水解可制得肥皂 | |
| B. | 在一定条件下,氨基酸之间能发生反应合成多肽 | |
| C. | 在淀粉水解液中加入氢氧化钠,再加入碘水,溶液未变蓝,说明淀粉己完全水解 | |
| D. | 蛋白质溶液中加入Na2SO4浓溶液有固体析出,加入足量水后固体不溶解 |
12.实验室里可按如图所示的装置干燥、储存气体 R,多余的气体可用水吸收,则 R是( )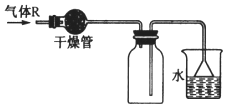

| A. | NO2 | B. | HCl | C. | SO2 | D. | NH3 |
13.对于某些离子的检验及结论一定正确的是( )
| A. | 加入硝酸银溶液产生白色沉淀,一定有Cl- | |
| B. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ | |
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ | |
| D. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |