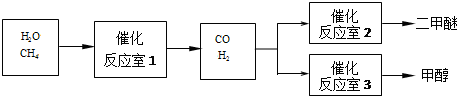
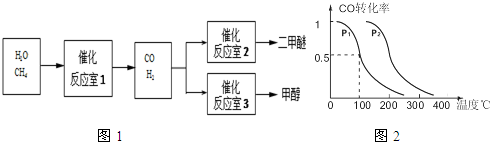
题目内容
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K= .
(2)该反应为 反应(填“吸热”或“放热”).
(3)能判断该反应是否达到化学平衡状态的依据是 (多选扣分).
A.容器中压强不变 B.混合气体中 c(CO)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)?c(H2)=c(CO)?c(H2O),试判断此时的温度为 ℃.
(5)某温度下,将CO和水蒸气各1mol置于密闭容器中反应,达到平衡后测得CO2为0.6mol,再通入4mol水蒸气,达到新的平衡后CO2的物质的量的范围是 .
其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=
(2)该反应为
(3)能判断该反应是否达到化学平衡状态的依据是
A.容器中压强不变 B.混合气体中 c(CO)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)?c(H2)=c(CO)?c(H2O),试判断此时的温度为
(5)某温度下,将CO和水蒸气各1mol置于密闭容器中反应,达到平衡后测得CO2为0.6mol,再通入4mol水蒸气,达到新的平衡后CO2的物质的量的范围是
考点:化学平衡常数的含义,化学平衡状态的判断
专题:化学平衡专题
分析:(1)依据化学方程式和平衡常数概念书写平衡常数;
(2)平衡常数随温度升温增大,说明平衡正向进行,结合平衡移动原理分析判断;
(3)平衡状态是正逆反应速率相同,各组分含量保持不变;
(4)依据平衡常数计算式和图表数据分析判断;
(5)反应CO+H2O(g)?CO2+H2达平衡后,加入水蒸气,化学平衡会向着正反应方向进行,但是反应物不可能全部转化为生成物.
(2)平衡常数随温度升温增大,说明平衡正向进行,结合平衡移动原理分析判断;
(3)平衡状态是正逆反应速率相同,各组分含量保持不变;
(4)依据平衡常数计算式和图表数据分析判断;
(5)反应CO+H2O(g)?CO2+H2达平衡后,加入水蒸气,化学平衡会向着正反应方向进行,但是反应物不可能全部转化为生成物.
解答:
解:(1)CO2(g)+H2(g)?CO(g)+H2O(g),反应的平衡常数K=
;
故答案为:
;
(2)图表中平衡常数随温度升高增大,说明升温平衡正向进行,正反应是吸热反应;
故答案为:吸热;
(3)A.反应前后气体体积不变,反应过程中和平衡状态压强不变,容器中压强不变不能说明费用达到平衡状态,故A错误;
B.混合气体中 c(CO)不变是平衡标志,故B正确;
C.反应速率之比等于化学方程式系数之比,是正反应速率之比,υ正(H2)=υ逆(H2O) 表面水的正逆反应速率相同,反应达到平衡状态,故C正确;
D.c(CO2)=c(CO)和起始量和消耗量有关,不能说明反应达到平衡状态,故D错误;
故答案为:BC.
(4)某温度下,平衡浓度符合下式:c(CO2)?c(H2)=c(CO)?c(H2O),K=1,依据图表数据可知,平衡常数随温度变化,温度不变,平衡常数不变,判断此时的温度为830°C;
故答案为:830;
(5)根据题意:CO+H2O(g)?CO2 +H2,
初始物质的量:1 1 0 0
变化物质的量:0.6 0.6 0.6 0.6
平衡物质的量:0.4 0.4 0.6 0.6
此时二氧化碳和氢气的物质的量之和是1.2mol,再通入4mol水蒸气,化学平衡会向着正反应方向进行,假设一氧化碳全部转化完毕,则会生成二氧化碳和氢气各0.4mol,此时CO2的物质的量1mol,但是一氧化碳不会全部转化,所以达到新的平衡后,CO2的物质的量介于0.6mol-1mol之间.
故答案为:0.6mol~1mol;
| c(CO)c(H2O) |
| c(CO2)c(H2) |
故答案为:
| c(CO)c(H2O) |
| c(CO2)c(H2) |
(2)图表中平衡常数随温度升高增大,说明升温平衡正向进行,正反应是吸热反应;
故答案为:吸热;
(3)A.反应前后气体体积不变,反应过程中和平衡状态压强不变,容器中压强不变不能说明费用达到平衡状态,故A错误;
B.混合气体中 c(CO)不变是平衡标志,故B正确;
C.反应速率之比等于化学方程式系数之比,是正反应速率之比,υ正(H2)=υ逆(H2O) 表面水的正逆反应速率相同,反应达到平衡状态,故C正确;
D.c(CO2)=c(CO)和起始量和消耗量有关,不能说明反应达到平衡状态,故D错误;
故答案为:BC.
(4)某温度下,平衡浓度符合下式:c(CO2)?c(H2)=c(CO)?c(H2O),K=1,依据图表数据可知,平衡常数随温度变化,温度不变,平衡常数不变,判断此时的温度为830°C;
故答案为:830;
(5)根据题意:CO+H2O(g)?CO2 +H2,
初始物质的量:1 1 0 0
变化物质的量:0.6 0.6 0.6 0.6
平衡物质的量:0.4 0.4 0.6 0.6
此时二氧化碳和氢气的物质的量之和是1.2mol,再通入4mol水蒸气,化学平衡会向着正反应方向进行,假设一氧化碳全部转化完毕,则会生成二氧化碳和氢气各0.4mol,此时CO2的物质的量1mol,但是一氧化碳不会全部转化,所以达到新的平衡后,CO2的物质的量介于0.6mol-1mol之间.
故答案为:0.6mol~1mol;
点评:本题考查学生可逆反应的特征以及化学平衡移动方面的知识,平衡常数计算,平衡标志分析是关键,注意知识的积累是解题的关键,难度不大.

练习册系列答案
相关题目
下列过程需要吸收热量的是( )
①水蒸气冷凝②煅烧石灰石③浓硫酸稀释④酸碱发生中和反应⑤生石灰跟水反应生成熟石灰⑥干冰升华⑦液氨汽化⑧水分解为氢气和氧气⑨氢原子两两结合为氢分子.
①水蒸气冷凝②煅烧石灰石③浓硫酸稀释④酸碱发生中和反应⑤生石灰跟水反应生成熟石灰⑥干冰升华⑦液氨汽化⑧水分解为氢气和氧气⑨氢原子两两结合为氢分子.
| A、①②⑤⑥⑨ | B、②③⑥⑨ |
| C、①④⑤⑦⑧ | D、②⑥⑦⑧ |
在0.1mol/L的NH3?H2O溶液中存在如下电离平衡:NH3?H2O?NH4++OH-对于该平衡,下列叙述正确的是( )
| A、加入少量NaOH固体,溶液中c(OH-)减少 |
| B、通入少量HCl气体,平衡向正反应方向移动 |
| C、加水,反应速率增大,平衡向逆反应方向移动 |
| D、加入少量NH4Cl固体,平衡向正反应方向移动 |
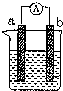 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题: