题目内容
写出下列各粒子的化学式
(1)由2个原子组成的具有10个电子的分子 阴离子是
(2)由4个原子组成的具有10个电子的分子是 阳离子是
(3)由3个原子组成的具有18个电子分子是
(4)由5个原子组成的具有10个电子的阳离子是 .
(1)由2个原子组成的具有10个电子的分子
(2)由4个原子组成的具有10个电子的分子是
(3)由3个原子组成的具有18个电子分子是
(4)由5个原子组成的具有10个电子的阳离子是
考点:质量数与质子数、中子数之间的相互关系
专题:原子组成与结构专题
分析:根据分子中电子数等于各原子的电子数之和;阳离子中电子数=质子数-电荷数;阴离子中电子数=质子数+电荷数;
解答:
解:(1)由2个原子组成的具有10个电子的分子为HF,阴离子是OH-;
故答案为:HF;OH-;
(2)由4个原子组成的具有10个电子的分子是NH3,阳离子是H3O+;
故答案为:NH3;H3O+;
(3)由3个原子组成的具有18个电子分子是H2S;
故答案为:H2S;
(4)由5个原子组成的具有10个电子的阳离子是NH4+;
故答案为:NH4+;
故答案为:HF;OH-;
(2)由4个原子组成的具有10个电子的分子是NH3,阳离子是H3O+;
故答案为:NH3;H3O+;
(3)由3个原子组成的具有18个电子分子是H2S;
故答案为:H2S;
(4)由5个原子组成的具有10个电子的阳离子是NH4+;
故答案为:NH4+;
点评:本题主要考查了常见的10电子、18电子微粒,难度不大,注意离子数目之间的关系,难度不大.

练习册系列答案
相关题目
已知:HCN(aq)+NaOH(aq)═NaCN(aq)+H2O(l)△H=-12.1kJ?mol-1;
HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H=-55.6kJ?mol-1
则HCN在水溶液中电离的△H等于( )
HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H=-55.6kJ?mol-1
则HCN在水溶液中电离的△H等于( )
| A、+43.5 kJ?mol-1 |
| B、+67.7 kJ?mol-1 |
| C、-43.5 kJ?mol-1 |
| D、-67.7 kJ?mol-1 |
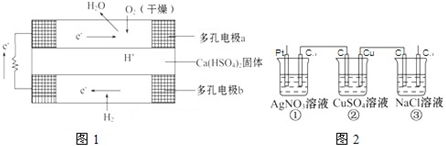
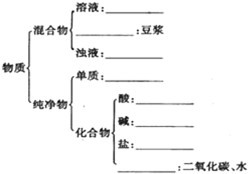 有下列物质:A.豆浆,B.食盐水,C.铁,D.硫酸,E.氢氧化钠固体,F.氯化钠,G.泥水,H.二氧化碳,I.水.请将它们的序号或所属类别填充到如图的横线上.(填写序号)
有下列物质:A.豆浆,B.食盐水,C.铁,D.硫酸,E.氢氧化钠固体,F.氯化钠,G.泥水,H.二氧化碳,I.水.请将它们的序号或所属类别填充到如图的横线上.(填写序号)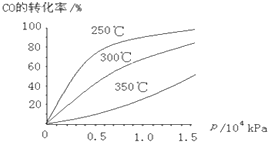 Ⅰ.一定温度下,将3mol CO2和2mol H2混合于2L的密闭容器中,发生如下反应:C02(g)+H2(g)?CO(g)+H2O(g)
Ⅰ.一定温度下,将3mol CO2和2mol H2混合于2L的密闭容器中,发生如下反应:C02(g)+H2(g)?CO(g)+H2O(g)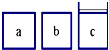 如图所示,相同体积的a、b、c三密闭容器,其中c容器有一活塞,a、b两容器为定容容器,起始向三容器中都加入相同量的SO2和O2使三容器压强相等,一定条件下发生2SO2+O2?2SO3的反应.问:
如图所示,相同体积的a、b、c三密闭容器,其中c容器有一活塞,a、b两容器为定容容器,起始向三容器中都加入相同量的SO2和O2使三容器压强相等,一定条件下发生2SO2+O2?2SO3的反应.问: