��Ŀ����
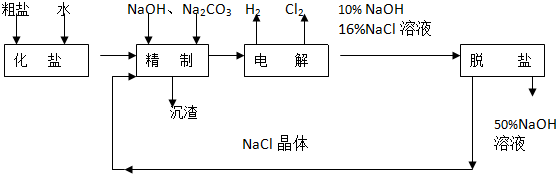
10���ҹ����ۼӵ�ʳ���к��е���أ���֪�������������������һ�ֽ�ǿ��������������⻯��������εȻ�ԭ�����ʷ�Ӧ����ҵ��������ص��������£�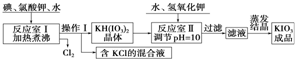
��ش��������⣺
��1����֪��Ӧ�Ң����ķ�Ӧ�У����ֻ�ԭ�������õ�������ͬ����д���÷�Ӧ�Ļ�ѧ����ʽ��6I2+11KClO3+3H2O=6KH��IO3��2+5KCl+3Cl2����
��2����Ӧ�Ң��������У���Ŀ���ǣ��ټӿ췴Ӧ���ʣ�ʹ��Ӧ���ַ�Ӧ���ڳ�ȥ��Ӧ���ɵ������������ڷ�Ӧ����Ӧ�������
����ӻ�ѧƽ��ǶȽ��ͣ���
��3����֪�������ʵ��ܽ�ȼ��±���
| KCl | KH��IO3��2 | KClO3 | |
| �ܽ��g/100gˮ��25�棩 | 20.8 | 0.8 | 7.5 |
| �ܽ��g/100gˮ��80�棩 | 37.1 | 12.4 | 16.2 |
��4���ڷ�Ӧ�Ң��м���KOH������Һ��pH=10����Ŀ����ʹKH��IO3��2ת��ΪKIO3��
��5����ͬѧ���ⶨ��Ʒ�е���صĺ��������������ʵ�飺
��ȷ��ȡ1g��Ʒ������������ˮʹ����ȫ�ܽ⣻
����ϡ�����ữ����������Һ���������KI��Һ����ֽ��裻
���Ե���Ϊָʾ������μ���2.0mol•L-1��Na2S2O3��Һ������ɫ�պ���ȥʱ������Na2S2O3��Һ12.00mL�����Ʒ��KIO3����������Ϊ85.6%����ʽ���㣬���������λ��Ч���֣�
����֪��KIO3+5KI+3H2SO4�T3K2SO4+3I2+3H2O��I2+2Na2S2O3�T2NaI+Na2S4O6����
��6����ͬѧ�ֶԴ�����NaCl������KIO3������������ʵ�飺
| �������� | ʵ������ |
| ȡ1g������NaCl����3mLˮ�����Һ�� | ��Һ�ޱ仯 |
| ����5�ε�����Һ��1mL 0.1mol/L KI��Һ���� | ��Һ�ޱ仯 |
| Ȼ���ٵ���1��1mol/L��H2SO4���� | ��Һ����ɫ |
�ڸ�����ͬѧ��ʵ�����Ʋ⣬��ͬѧ��ʵ������ƫ���ƫ����ƫС������Ӱ�족����
���� ��1����Ӧ��I2��KH��IO3��2��IԪ�ػ��ϼ���0������Ϊ+5�ۣ�������10�ۣ�KClO3��KCl��Cl2����Ԫ�ػ��ϼ۽��ͣ���ԭ����ΪKCl��Cl2��KClO3��KCl��Ԫ�ػ��ϼ���+5����Ϊ-1�ۣ����ϼ۽���6�ۣ�KClO3��Cl2��Ԫ�ػ��ϼ���+5����Ϊ0�ۣ����ϼ��ܹ�����10�ۣ�����õĵ�����Ŀ��ͬ����õ�����С������Ϊ30����KCl��ϵ��Ϊ5��Cl2��ϵ��Ϊ3�����Ի��ϼ۽���60�ۣ���I2ϵ��Ϊ6������Ԫ���غ���ƽKClO3��H2O��KH��IO3��2��ϵ����
��2��������мӿ췴Ӧ���ʣ���ȥ���ɵ�������ƽ��������У�
��3�������ݷ�����֪KH��IO3��2�ڳ������ܽ��С��
��4��KH��IO3��2�ڼ��������¿���ת����KHIO3���������ʵ��ܽ�ȿ���ȷ����Һ��þ���ķ�����
��5��������������������صĹ�ϵʽ�������ص����ʵ������ٸ�������������ʽ�������صĺ�����
��6�����������£������ӱ������������ɵⵥ�ʣ������ĵ������ױ������������ɵⵥ�ʣ�
��� �⣺��1����Ӧ��I2��KH��IO3��2��IԪ�ػ��ϼ���0������Ϊ+5�ۣ�������10�ۣ�KClO3��KCl��Cl2����Ԫ�ػ��ϼ۽��ͣ���ԭ����ΪKCl��Cl2��KClO3��KCl��Ԫ�ػ��ϼ���+5����Ϊ-1�ۣ����ϼ۽���6�ۣ�KClO3��Cl2��Ԫ�ػ��ϼ���+5����Ϊ0�ۣ����ϼ��ܹ�����10�ۣ�����õĵ�����Ŀ��ͬ����õ�����С������Ϊ30����KCl��ϵ��Ϊ5��Cl2��ϵ��Ϊ3�����Ի��ϼ۽���60�ۣ���I2ϵ��Ϊ6��������Ԫ���غ��֪KClO3ϵ��Ϊ11�����ݵ�Ԫ���غ��֪KH��IO3��2��ϵ��Ϊ6��������Ԫ���غ��֪H2O��ϵ��Ϊ3�������Ԫ���غ㣬�ʷ���ʽΪ��6I2+11KClO3+3H2O=6KH��IO3��2+5KCl+3Cl2����
�ʴ�Ϊ��6I2+11KClO3+3H2O=6KH��IO3��2+5KCl+3Cl2����
��2����Ӧ�Ң��������У���Ŀ���ǣ��ټӿ췴Ӧ���ʣ�ʹ��Ӧ���ַ�Ӧ��ȥ��Ӧ���ɵ������������ڷ�Ӧ����Ӧ������У�
�ʴ�Ϊ����ȥ��Ӧ���ɵ������������ڷ�Ӧ����Ӧ������У�
��3�������ݷ�����֪KH��IO3��2�ڳ������ܽ��С���������ǵõ�KH��IO3��2���壬����������Ϊ����ȴ�ᾧ�����˵õ����壬
�ʴ�Ϊ����ȴ�ᾧ�����ˣ�
��4��KH��IO3��2�ڼ��������¿���ת����KHIO3�����Բ�����е���pH=10��Ŀ����ʹKH��IO3��2ת��ΪKIO3������KIO3���ܽ�����¶ȵ�Ӱ��ϴ��ҷֽ��¶Ƚϸߣ����Բ�ȡ�����ᾧ�ķ�����
�ʴ�Ϊ��ʹKH��IO3��2ת��ΪKIO3��
��5�������ص����ʵ���Ϊx��
KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O�٣� I2+2S2O3 2-=2I-+S4 O62-�ڣ�������ʽ�ڡ�3+�ٵ�
IO3+6H++6S2O32-=I-+3S4O62-+3H2O
1 6
x 2.0mol/L��0.012L
x=0.004mol������ص�����=0.004mol��214g/mol=0.856g�����Ե���ص���������=$\frac{0.856g}{1g}$��100%=85.6%��
�ʴ�Ϊ��85.6%��
��6�����������£������ӱ������������ɵⵥ�ʣ����ӷ�Ӧ����ʽΪ��4I-+4H++O2=2I2+2H2O��
�����������£������ĵ������ױ������������������ɵⵥ�ʣ����²ⶨ���ƫ��
�ʴ�Ϊ��4I-+4H++O2=2I2+2H2O��ƫ��
���� ������һ�����ʷ�����ᴿ�Լ��к͵ζ�֪ʶ���ۺ�ʵ���⣬Ҫ��ѧ������֪ʶǨ�ƺ�Ӧ�õ���������Ŀ�Ѷ��еȣ�

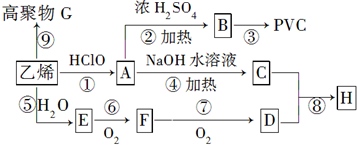
| A�� | ȼ�շ� | B�� | ���� | C�� | ������� | D�� | �˴Ź������� |
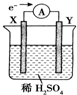 ��ͼ����ʢ��ϡH2SO4���ձ��з����õ������ӵĵ缫X��Y�����·�е���������ͼ��ʾ�����ڸ�װ�õ�����˵����ȷ���ǣ�������
��ͼ����ʢ��ϡH2SO4���ձ��з����õ������ӵĵ缫X��Y�����·�е���������ͼ��ʾ�����ڸ�װ�õ�����˵����ȷ���ǣ�������| A�� | ��Һ�У�SO42-��Y���ƶ� | |
| B�� | �����缫�ֱ�Ϊ����̼������XΪ̼����YΪ�� | |
| C�� | X���Ϸ������ǻ�ԭ��Ӧ��Y���Ϸ�������������Ӧ | |
| D�� | �����缫���ǽ����������ǵĻ��˳��ΪX��Y |
| A�� | Һ̬HBr�����磬���HBr�Ƿǵ���� | |
| B�� | ǿ�������Һ�ĵ����Բ�һ����ǿ | |
| C�� | NH3��ˮ��Һ�ܵ��磬���NH3�ǵ���� | |
| D�� | ǿ�������Һ̬ʱһ���ܵ��� |
| A�� | �������ƺ�ˮ��Ӧ��2Na2O2+2 H2O=4Na++4OH-+O2�� | |
| B�� | ��������������������Һ��Al2O3+2 OH-=2AlO2-+H2�� | |
| C�� | ����������Һ����ϡ�����У�Ba2++OHһ+H++SO42-=BaSO4��+H2O | |
| D�� | ������̼ͨ����������������Һ��CO2+OH-=HCO3- |
 ��
��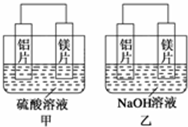 �мס�����λͬѧ��������ԭ��ط�Ӧ�������Ļ��˳�����˾���þƬ����Ƭ���缫������ͬѧ���缫����6mol•L-1��H2SO4��Һ�У���ͬѧ���缫����6mol•L-1��NaOH��Һ�У���ͼ��ʾ��
�мס�����λͬѧ��������ԭ��ط�Ӧ�������Ļ��˳�����˾���þƬ����Ƭ���缫������ͬѧ���缫����6mol•L-1��H2SO4��Һ�У���ͬѧ���缫����6mol•L-1��NaOH��Һ�У���ͼ��ʾ��