题目内容
15.下列叙述中正确的是( )| A. | 液态HBr不导电,因此HBr是非电解质 | |
| B. | 强电解质溶液的导电性不一定很强 | |
| C. | NH3的水溶液能导电,因此NH3是电解质 | |
| D. | 强电解质在液态时一定能导电 |
分析 A.依据非电解质是指:在熔融状态和水溶液中都不能导电的化合物判断;
B.根据强电解质与溶液的导电性的关系分析解答;
C.电解质是指:在水溶液中或熔融状态下能够导电的化合物.电解质水溶液中或熔融状态下能够导电,是因电解质自身可以离解成自由移动的离子;
D.共价化合物的强电解质在液态时一定不能导电.
解答 解:A.液态HBr没有自由移动的离子不导电,但液态HBr在水中能完全电离导电,所以HBr是电解质,故A错误;
B.强电解质与电解质是否完全电离有关,导电性与溶液中离子浓度有关,所以强电解质溶液的导电性不一定很强,如硫酸钡难溶于水溶液导电性不强,但它是强电解质,乙酸易溶于水导电性强,但它是弱酸,故B正确;
C.氨气的水溶液能导电,但电离出阴阳离子的物质是一水合氨而不是氨气,因此NH3是非电解质,故C错误;
D.强电解质在液态时不一定能导电,如共价化合物HBr,液态没有自由移动的离子只有分子不导电,故D错误;
故选B.
点评 本题重点考查了电解质、非电解质概念的辨析、电解质与导电的关系的判断,注意电解质必须是化合物,电解质导电是存在自由移动的离子,题目难度不大.

练习册系列答案
相关题目
6.已知反应X+Y=M+N为吸热反应,对这个反应的下列说法中正确的是( )
| A. | X和Y的总能量一定低于M和N的总能量 | |
| B. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| C. | 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 | |
| D. | X的能量一定低于M的,Y的能量一定低于N的 |
3.十二届全国人民代表大会政府工作报告中强调“加强雾霾治理,淘汰黄标车和老旧车”,下列物质不属于空气污染物的是( )
| A. | CO2 | B. | SO2 | C. | NO2 | D. | PM2.5 |
10.我国市售加碘食盐中含有碘酸钾.已知碘酸钾在酸性条件下是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应.工业生产碘酸钾的流程如下:
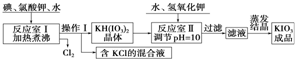
请回答下列问题:
(1)已知反应室Ⅰ发生的反应中,两种还原产物所得电子数相同,请写出该反应的化学方程式:6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑.
(2)反应室Ⅰ需加热煮沸,其目的是:①加快反应速率,使反应物充分反应:②除去反应生成的氯气,有利于反应正反应方向进行
(请从化学平衡角度解释).
(3)已知几种物质的溶解度见下表:
由上表数据分析可知,操作Ⅰ的名称为冷却结晶、过滤.
(4)在反应室Ⅱ中加入KOH调节溶液的pH=10,其目的是使KH(IO3)2转化为KIO3.
(5)甲同学欲测定成品中碘酸钾的含量,设计了如下实验:
①准确称取1g样品,加适量蒸馏水使其完全溶解;
②用稀硫酸酸化上述所得溶液,加入过量KI溶液,充分搅拌;
③以淀粉为指示剂,逐滴加入2.0mol•L-1的Na2S2O3溶液,当蓝色刚好褪去时,消耗Na2S2O3溶液12.00mL,则成品中KIO3的质量分数为85.6%(列式计算,结果保留三位有效数字)
(已知:KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O,I2+2Na2S2O3═2NaI+Na2S4O6).
(6)乙同学又对纯净的NaCl(不含KIO3)进行了下列实验:
①请推测实验中产生蓝色现象的可能原因,用离子方程式表示4I-+4H++O2=2I2+2H2O.
②根据乙同学的实验结果推测,甲同学的实验结果会偏大(填“偏大”,“偏小”或“无影响”).

请回答下列问题:
(1)已知反应室Ⅰ发生的反应中,两种还原产物所得电子数相同,请写出该反应的化学方程式:6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑.
(2)反应室Ⅰ需加热煮沸,其目的是:①加快反应速率,使反应物充分反应:②除去反应生成的氯气,有利于反应正反应方向进行
(请从化学平衡角度解释).
(3)已知几种物质的溶解度见下表:
| KCl | KH(IO3)2 | KClO3 | |
| 溶解度g/100g水(25℃) | 20.8 | 0.8 | 7.5 |
| 溶解度g/100g水(80℃) | 37.1 | 12.4 | 16.2 |
(4)在反应室Ⅱ中加入KOH调节溶液的pH=10,其目的是使KH(IO3)2转化为KIO3.
(5)甲同学欲测定成品中碘酸钾的含量,设计了如下实验:
①准确称取1g样品,加适量蒸馏水使其完全溶解;
②用稀硫酸酸化上述所得溶液,加入过量KI溶液,充分搅拌;
③以淀粉为指示剂,逐滴加入2.0mol•L-1的Na2S2O3溶液,当蓝色刚好褪去时,消耗Na2S2O3溶液12.00mL,则成品中KIO3的质量分数为85.6%(列式计算,结果保留三位有效数字)
(已知:KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O,I2+2Na2S2O3═2NaI+Na2S4O6).
(6)乙同学又对纯净的NaCl(不含KIO3)进行了下列实验:
| 操作步骤 | 实验现象 |
| 取1g纯净的NaCl,加3mL水配成溶液. | 溶液无变化 |
| 滴入5滴淀粉溶液和1mL 0.1mol/L KI溶液,振荡. | 溶液无变化 |
| 然后再滴入1滴1mol/L的H2SO4,振荡. | 溶液变蓝色 |
②根据乙同学的实验结果推测,甲同学的实验结果会偏大(填“偏大”,“偏小”或“无影响”).
20.下列各组微粒中,核外电子排布相同的是( )
| A. | F-Cl -Na+ | B. | O2-S2-Cl- | C. | S2-Cl-Na+ | D. | Ne Mg2+Al3+ |
7.下列各组分子中,中心原子杂化轨道的类型不相同的是( )
| A. | CO2与SO2 | B. | CH4与NH3 | C. | SO3与BF3 | D. | H2S与CCl4 |
4.下列离子方程式书写错误的是( )
| A. | 铝粉投入到NaOH溶液中:2Al+6H2O+2OH-=2[Al(OH)4]-+3H2↑ | |
| B. | 往Al(OH)3中滴加氨水:Al(OH)3+OH-=[Al(OH)4]- | |
| C. | 向水玻璃中通入少量二氧化碳:SiO32-+CO2+H2O=H2SiO3↓+CO32- | |
| D. | Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-+3H2O=2[Al(OH)4]- |