题目内容
CaO2?8H2O呈白色,微溶于水,加热至350℃左右开始分解放出氧气,425℃分解完全.过氧化钙可以用于改善地表水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等.实验室先用大理石(含MgCO3、FeCO3等杂质)制取纯净的碳酸钙,然后再用纯的碳酸钙制取过氧化钙.实验流程如下:
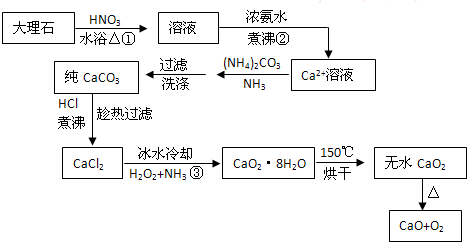
已知:Ca(OH)2+H2O2+6H2O=CaO2?8H2O△H<0
(1)写出CaO2的电子式: .
(2)步骤②中加入浓氨水至弱碱性的目的是: .
(3)步骤③发生反应的化学方程式为: .
(4)步骤③用冰水冷却的原因除了减少H2O2的分解以外还有 .

已知:Ca(OH)2+H2O2+6H2O=CaO2?8H2O△H<0
(1)写出CaO2的电子式:
(2)步骤②中加入浓氨水至弱碱性的目的是:
(3)步骤③发生反应的化学方程式为:
(4)步骤③用冰水冷却的原因除了减少H2O2的分解以外还有
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:(1)CaO2是过氧根离子和钙离子通过离子键形成的离子化合物,据此书写电子式;
(2)硝酸镁、硝酸铁可以喝氨水发生复分解反应,形成氢氧化镁、氢氧化铁沉淀;
(3)根据流程图知道:氯化钙的水溶液,加入双氧水、氨气,冰水冷却,可以得到CaO2?8H2O;
(4)根据高温下双氧水以及CaO2?8H2O的性质来回答.
(2)硝酸镁、硝酸铁可以喝氨水发生复分解反应,形成氢氧化镁、氢氧化铁沉淀;
(3)根据流程图知道:氯化钙的水溶液,加入双氧水、氨气,冰水冷却,可以得到CaO2?8H2O;
(4)根据高温下双氧水以及CaO2?8H2O的性质来回答.
解答:
解:大理石(含MgCO3、FeCO3等杂质)制取纯净的碳酸钙,然后再用纯的碳酸钙制取过氧化钙的原理:大理石(含MgCO3、FeCO3等杂质)都可以和硝酸之间发生反应得到硝酸钙、硝酸镁以及硝酸铁的混合物用,FeCO3与硝酸反应是氧化还原反应,向混合液中加入氨水,可以形成氢氧化镁、氢氧化铁沉淀,过滤,得到的滤液是硝酸钙溶液(含铵根离子),向其中加入碳酸铵,发生复分解反应,可以得到碳酸钙沉淀,沉淀用盐酸溶解,得到氯化钙的水溶液,加入双氧水、氨气,冰水冷却,可以得到CaO2?8H2O,低温下烘干,可以得到CaO2,进一步加热可以得到氧化钙和氧气.
(1)CaO2是过氧根离子和钙离子通过离子键形成的离子化合物,电子式为: ,故答案为:
,故答案为: ;
;
(2)硝酸钙、硝酸镁以及硝酸铁的混合物中加入氨水,可以形成氢氧化镁、氢氧化铁沉淀,故答案为:使其中Mg2+、Fe3+等杂质离子形成沉淀除去;
(3)氯化钙的水溶液,加入双氧水、氨气,冰水冷却,可以得到CaO2?8H2O,该反应的反应物为CaCl2、H2O2、NH3,故方程式为CaCl2+H2O2+2NH3+8H2O=CaO2?8H2O+2NH4Cl,故答案为:CaCl2+H2O2+2NH3+8H2O=CaO2?8H2O+2NH4Cl;
(4)因为H2O2受热易分解,故采用冰水冷却的方式防止其分解,提高利用率,同时温度低能降低物质的溶解度,提高产率,故答案为:该反应是放热反应,温度低有利于提高CaO2?8H2O产率.
(1)CaO2是过氧根离子和钙离子通过离子键形成的离子化合物,电子式为:
 ,故答案为:
,故答案为: ;
;(2)硝酸钙、硝酸镁以及硝酸铁的混合物中加入氨水,可以形成氢氧化镁、氢氧化铁沉淀,故答案为:使其中Mg2+、Fe3+等杂质离子形成沉淀除去;
(3)氯化钙的水溶液,加入双氧水、氨气,冰水冷却,可以得到CaO2?8H2O,该反应的反应物为CaCl2、H2O2、NH3,故方程式为CaCl2+H2O2+2NH3+8H2O=CaO2?8H2O+2NH4Cl,故答案为:CaCl2+H2O2+2NH3+8H2O=CaO2?8H2O+2NH4Cl;
(4)因为H2O2受热易分解,故采用冰水冷却的方式防止其分解,提高利用率,同时温度低能降低物质的溶解度,提高产率,故答案为:该反应是放热反应,温度低有利于提高CaO2?8H2O产率.
点评:本题考查了制备实验方案的设计,该题是高考中的常见考点和题型,属于中等难度试题的考查,试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和规范严谨的实验设计能力,提高学生的学科素养.该题的关键是明确物质的性质及发生的化学反应,并能灵活运用即可.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
如果a g某气体中含有该气体的分子数为b,则cg该气体在标准状况下的体积是(各选项中NA为阿伏加德罗常数的值)( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列叙述不正确的是( )
| A、碳酸钙能够溶解在二氧化碳的水溶液中 |
| B、氢氧化镁可溶于盐酸不溶于氯化铵溶液 |
| C、氯化银可溶于氨水 |
| D、硫酸镁溶液中滴加氢氧化钡得到两种沉淀 |
将10mL N2和H2的混合气体在催化剂作用下,500℃左右发生下列可逆反应左右发生下列可逆反应:N2(g)+3H2(g)?2NH3(g),已知反应达到平衡后在相同条件下混合气体体积变为6mL,则在原混合气体中,N2和H2的物质的量之比可能是( )
| A、2:3 | B、1:3 |
| C、1:4 | D、1:7 |
用于净化汽车尾气的反应:2NO(g)+2CO(g)?2CO2(g)+N2(g),已知该反应在570K时几乎完全反应,但反应速率极慢.下列说法正确的是( )
| A、装有尾气净化装置的汽车排出的气体中不再含有NO或CO |
| B、提高尾气净化效率的常用方法是升高温度 |
| C、增大压强,上述平衡右移,故可通过增压的方法提高尾气净化效率 |
| D、提高尾气净化效率的最佳途径是使用高效催化剂 |
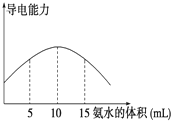 电离度是描述弱电解质电离程度的物理量,电离度=(已电离的电解质的物质的量/原来总的物质的量)×100%.现取20mL pH=3的 CH3COOH溶液,加入0.2mol?L-1的氨水,测得溶液导电性变化如图,则加入氨水前CH3COOH的电离度为( )
电离度是描述弱电解质电离程度的物理量,电离度=(已电离的电解质的物质的量/原来总的物质的量)×100%.现取20mL pH=3的 CH3COOH溶液,加入0.2mol?L-1的氨水,测得溶液导电性变化如图,则加入氨水前CH3COOH的电离度为( )| A、0.5% | B、1.5% |
| C、0.1% | D、1% |
下列说法正确的是( )
| A、分子晶体中一定不含离子键,但一定存在共价键 |
| B、金属与非金属元素形成的化合物一定是离子化合物 |
| C、NCl3分子中所有的原子均为8电子稳定结构 |
| D、NaHSO4晶体中阴、阳离子的个数比是1:2 |
短周期元素W、X、Y、Z的原子序数依次增大,下列相关比较错误的是( )
| A、稳定性:H2X<H2Z |
| B、酸性:H2YO3<HZO4 |
| C、还原性:W-<Z2- |
| D、半径:Y3+<Z2- |
 ,A及有机物的关系为:
,A及有机物的关系为: