题目内容
下列说法正确的是( )
| A、分子晶体中一定不含离子键,但一定存在共价键 |
| B、金属与非金属元素形成的化合物一定是离子化合物 |
| C、NCl3分子中所有的原子均为8电子稳定结构 |
| D、NaHSO4晶体中阴、阳离子的个数比是1:2 |
考点:化学键,原子核外电子排布,离子化合物的结构特征与性质
专题:
分析:A、分子晶体中一定不含离子键,单原子分子中不含共价键;
B、氯化铝是由金属与非金属元素形成的共价化合物;
C、在ABn型分子中,如果A原子的族序数+成键原子个数=8,则该分子中所有原子都达到8电子稳定结构;
D、NaHSO4晶体中含有一个钠离子和一个硫酸氢根离子.
B、氯化铝是由金属与非金属元素形成的共价化合物;
C、在ABn型分子中,如果A原子的族序数+成键原子个数=8,则该分子中所有原子都达到8电子稳定结构;
D、NaHSO4晶体中含有一个钠离子和一个硫酸氢根离子.
解答:
解:A、分子晶体中一定不含离子键,单原子分子中不含共价键,如稀有气体单质分子为单原子分子,分子中没有共价键,故A错误;
B、金属与非金属元素形成的化合物不一定是离子化合物,如氯化铝是由金属与非金属元素形成的共价化合物,故B错误;
C、NCl3分子中,中N原子最外层有5个电子,化合价是+3价,所以达到8电子稳定结构;氯原子最外层有7个电子,化合价的绝对值是1,所以达到8电子稳定结构,故C正确;
D、NaHSO4晶体中含有一个钠离子和一个硫酸氢根离子,所以NaHSO4晶体中阴、阳离子的个数比是1:1,离子晶体在熔化时,只破坏离子键,故D错误.
故选C.
B、金属与非金属元素形成的化合物不一定是离子化合物,如氯化铝是由金属与非金属元素形成的共价化合物,故B错误;
C、NCl3分子中,中N原子最外层有5个电子,化合价是+3价,所以达到8电子稳定结构;氯原子最外层有7个电子,化合价的绝对值是1,所以达到8电子稳定结构,故C正确;
D、NaHSO4晶体中含有一个钠离子和一个硫酸氢根离子,所以NaHSO4晶体中阴、阳离子的个数比是1:1,离子晶体在熔化时,只破坏离子键,故D错误.
故选C.
点评:本题考查晶体的组成、化合物的分类、8电子稳定结构的判断,题目难度不大,注意掌握8电子稳定结构的判断方法.

练习册系列答案
 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案
相关题目
下列有关实验装置的说法中正确的是( )
A、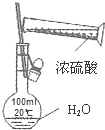 配制1.00mol/L的稀硫酸 |
B、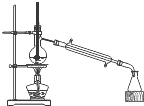 可以从I2的CCl4溶液中得到碘 |
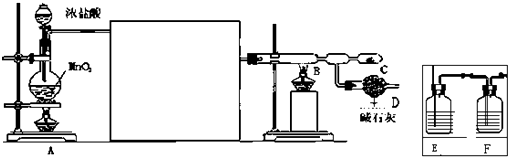
C、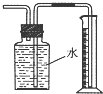 可测量Cu 与浓硝酸反应产生气体的体积 |
D、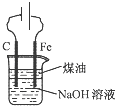 可用于实验室制备Fe (OH)2 |
在强碱性溶液中能大量共存的离子组是( )
| A、Na+、NH4+、H+、NO3- |
| B、K+、Ca2+、HCO3-、NO3- |
| C、Na+、Mg2+、Cl-、NO3- |
| D、Na+、Ba2+、NO3-、Cl- |
加入适当的氧化剂才能实现下列变化的是( )
| A、Fe2+→Fe3+ |
| B、S2-→H2S |
| C、MnO4-→Mn2+ |
| D、AlO2-→Al3+ |
 一定温度压强下,用m g的CH4、CO2、O2、SO2四种气体分别吹出四个体积大小不同的气球,下列说法中正确的是( )
一定温度压强下,用m g的CH4、CO2、O2、SO2四种气体分别吹出四个体积大小不同的气球,下列说法中正确的是( )| A、气球B中装的是O2 |
| B、气球A和气球C中气体分子数相等 |
| C、气球A和气球D中气体物质的量之比为4:1 |
| D、气球C和气球D中气体密度之比为2:1 |