题目内容
氯化铜、氯化亚铜是重要的化工原料,广泛地用作有机合成催化剂.
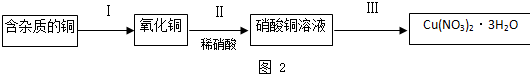
实验室中以粗铜(含杂质Fe)为原料,某种制备铜的氯化物的流程如下.

按要求回答下列问题:
(1)操作①的名称是 ,检验溶液2中是否含有杂质离子的试剂是 .操作②需在氯化氢气流中经过加热浓缩、 、过滤、洗涤、干燥.
(2)上述流程中,所得固体1需要加稀盐酸溶解,其理由是 ;溶液1可加试剂X用于调节pH以除去杂质,X可选用下列试剂中的(填序号) .
a.NaOH b.NH3?H2O c.CuO d.CuSO4
(3)反应②是向溶液2中通入一定量的SO2,加热一段时间后生成CuCl白色沉淀.写出制备CuCl的离子方程式: .
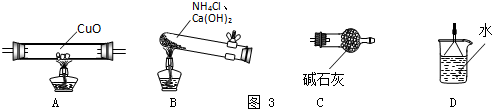
(4)现用如图所示的实验仪器及药品来制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹省略).

①按气流方向连接各仪器接口顺序是:a→ 、 → 、 → 、 → .实验开始前要进行一步重要操作,其操作名称是 .
②反应时,盛粗铜粉的试管中的现象是 .
③反应后,盛有NaOH溶液的广口瓶中溶液具有漂白、消毒作用,若用钢铁(含Fe、C)制品盛装该溶液会发生电化腐蚀,钢铁制品表面生成红褐色沉淀,溶液会失去漂白、杀菌消毒功效.该电化腐蚀过程中的正极反应式为 .
实验室中以粗铜(含杂质Fe)为原料,某种制备铜的氯化物的流程如下.

按要求回答下列问题:
(1)操作①的名称是
(2)上述流程中,所得固体1需要加稀盐酸溶解,其理由是
a.NaOH b.NH3?H2O c.CuO d.CuSO4
(3)反应②是向溶液2中通入一定量的SO2,加热一段时间后生成CuCl白色沉淀.写出制备CuCl的离子方程式:
(4)现用如图所示的实验仪器及药品来制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹省略).

①按气流方向连接各仪器接口顺序是:a→
②反应时,盛粗铜粉的试管中的现象是
③反应后,盛有NaOH溶液的广口瓶中溶液具有漂白、消毒作用,若用钢铁(含Fe、C)制品盛装该溶液会发生电化腐蚀,钢铁制品表面生成红褐色沉淀,溶液会失去漂白、杀菌消毒功效.该电化腐蚀过程中的正极反应式为
考点:制备实验方案的设计,铜金属及其重要化合物的主要性质
专题:实验题
分析:粗铜(含杂质Fe)与氯气反应生成氯化铁和氯化铜,加稀盐酸溶解,形成氯化铁和氯化铜溶液,再加CuO或氢氧化铜等调节pH,使铁离子转化为氢氧化铁沉淀,过滤得到的固体2为氢氧化铁,溶液2为氯化铜溶液,通入二氧化硫,二氧化硫与铜离子发生氧化还原反应生成CuCl,氯化铜溶液在HCl氛围中蒸发结晶得到CuCl2?2H2O;
(1)操作①是分离固体和液体混合物的操作;溶液2中若含有杂质离子则是Fe3+,用KSCN溶液检验;根据从溶液中提取溶质晶体的操作分析;
(2)氯化铜、氯化铁中的金属离子易水解,加入过量的酸可以抑制氯化铜、氯化铁水解;用于调节pH以除去溶液1杂质可加试剂具有与酸反应,且不引入Cu2+之外的离子;
(3)根据信息可知:SO2与铜离子反应生成CuCl白色沉淀和SO42-;
(4)①仪器连接顺序:Cl2发生装置→除去HCl气体装置→干燥装置→制备装置→多余Cl2处理装置;实验前要检验装置的气密性;
②Cu与Cl2反应产生大量棕黄色烟(CuCl2);
③正极上ClO-得电子生成Cl-.
(1)操作①是分离固体和液体混合物的操作;溶液2中若含有杂质离子则是Fe3+,用KSCN溶液检验;根据从溶液中提取溶质晶体的操作分析;
(2)氯化铜、氯化铁中的金属离子易水解,加入过量的酸可以抑制氯化铜、氯化铁水解;用于调节pH以除去溶液1杂质可加试剂具有与酸反应,且不引入Cu2+之外的离子;
(3)根据信息可知:SO2与铜离子反应生成CuCl白色沉淀和SO42-;
(4)①仪器连接顺序:Cl2发生装置→除去HCl气体装置→干燥装置→制备装置→多余Cl2处理装置;实验前要检验装置的气密性;
②Cu与Cl2反应产生大量棕黄色烟(CuCl2);
③正极上ClO-得电子生成Cl-.
解答:
解:粗铜(含杂质Fe)与氯气反应生成氯化铁和氯化铜,加稀盐酸溶解,形成氯化铁和氯化铜溶液,再加CuO或氢氧化铜等调节pH,使铁离子转化为氢氧化铁沉淀,过滤得到的固体2为氢氧化铁,溶液2为氯化铜溶液,通入二氧化硫,二氧化硫与铜离子发生氧化还原反应生成CuCl,氯化铜溶液在HCl氛围中蒸发结晶得到CuCl2?2H2O;
(1)操作①是分离固体和液体混合物的操作为过滤;溶液2中若含有杂质离子则是Fe3+,用KSCN溶液检验Fe3+;CuCl2易水解在氯化氢气流中经过加热浓缩、冷却结晶、过滤、洗涤、干燥;
故答案为:过滤;KSCN溶液;冷却结晶;
(2)氯化铜、氯化铁中的金属离子易水解,直接用水溶液配制溶液会产生浑浊,所以加入过量的酸来溶解氯化铜、氯化铁,以抑制氯化铜、氯化铁水解;用于调节pH以除去溶液1杂质可加试剂具有与酸反应,且不引入Cu2+之外的离子,故用CuO或Cu2(OH)或Cu2(OH)2CO3;
故答案为:抑制氯化铜、氯化铁水解;c;
(3)根据信息可知:在加热条件下,SO2与铜离子反应生成CuCl白色沉淀和SO42-,其反应的离子方程式为:2Cu2++2Cl-+SO2+2H2O
2CuCl↓+4H++SO42-;
故答案为:2Cu2++2Cl-+SO2+2H2O
2CuCl↓+4H++SO42-;
(4)①仪器连接顺序:Cl2发生装置→除去HCl气体装置→干燥装置→制备装置→多余Cl2处理装置,所以各仪器接口顺序是:a→d、e→j、h→f、g→b;该实验中有有毒气体参加反应,所以实验前要检验装置的气密性;
故答案为:d、e,j、h,f、g,b;检查装置的气密性;
②Cu与Cl2反应产生大量棕黄色烟(CuCl2),则反应时盛粗铜粉的试管中的现象是产生大量棕黄色烟;
故答案为:产生大量棕黄色烟;
③反应后,盛有NaOH溶液的广口瓶中生成NaClO溶液,该溶液具有漂白、消毒作用,若用钢铁(含Fe、C)制品盛装该溶液会发生电化腐蚀,ClO-得电子作正极生成Cl-,则正极上的电极方程式为:ClO-+2e-+H2O=Cl-+2OH-,
故答案为:ClO-+2e-+H2O=Cl-+2OH-.
(1)操作①是分离固体和液体混合物的操作为过滤;溶液2中若含有杂质离子则是Fe3+,用KSCN溶液检验Fe3+;CuCl2易水解在氯化氢气流中经过加热浓缩、冷却结晶、过滤、洗涤、干燥;
故答案为:过滤;KSCN溶液;冷却结晶;
(2)氯化铜、氯化铁中的金属离子易水解,直接用水溶液配制溶液会产生浑浊,所以加入过量的酸来溶解氯化铜、氯化铁,以抑制氯化铜、氯化铁水解;用于调节pH以除去溶液1杂质可加试剂具有与酸反应,且不引入Cu2+之外的离子,故用CuO或Cu2(OH)或Cu2(OH)2CO3;
故答案为:抑制氯化铜、氯化铁水解;c;
(3)根据信息可知:在加热条件下,SO2与铜离子反应生成CuCl白色沉淀和SO42-,其反应的离子方程式为:2Cu2++2Cl-+SO2+2H2O
| ||
故答案为:2Cu2++2Cl-+SO2+2H2O
| ||
(4)①仪器连接顺序:Cl2发生装置→除去HCl气体装置→干燥装置→制备装置→多余Cl2处理装置,所以各仪器接口顺序是:a→d、e→j、h→f、g→b;该实验中有有毒气体参加反应,所以实验前要检验装置的气密性;
故答案为:d、e,j、h,f、g,b;检查装置的气密性;
②Cu与Cl2反应产生大量棕黄色烟(CuCl2),则反应时盛粗铜粉的试管中的现象是产生大量棕黄色烟;
故答案为:产生大量棕黄色烟;
③反应后,盛有NaOH溶液的广口瓶中生成NaClO溶液,该溶液具有漂白、消毒作用,若用钢铁(含Fe、C)制品盛装该溶液会发生电化腐蚀,ClO-得电子作正极生成Cl-,则正极上的电极方程式为:ClO-+2e-+H2O=Cl-+2OH-,
故答案为:ClO-+2e-+H2O=Cl-+2OH-.
点评:本题以实验室制备氯化铜为背景,考查了物质的制备实验操作、离子检验、除杂质、离子方程式的书写、原电池原理的应用等,题目涉及的知识点较多,侧重于基础知识的综合应用的考查.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
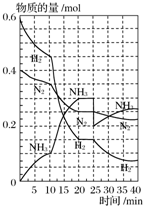 500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3的物质的量变化如图所示,下列说法中正确的是( )
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3的物质的量变化如图所示,下列说法中正确的是( )| A、从反应开始到第一次平衡时,N2的平均反应速率为0.005 mol?L-1?min-1 |
| B、平衡在10 min至20 min的变化,可能是因为增大了容器体积 |
| C、25 min时,分离出了0.1 mol NH3 |
| D、在25 min后平衡向正反应方向移动,新平衡中NH3的体积分数比原平衡的小 |
下列说法正确的是( )
| A、电解质在水中一定能导电 |
| B、纯水的导电性很差,所以水不是电解质 |
| C、溶液导电性的强弱取决于溶液中离子浓度及所带电荷的多少 |
| D、NaCl溶液在电流作用下电离成Na+与Cl- |
下列说法正确的是( )
| A、常温下醋酸分子不可能存在于pH>7的碱性溶液中 |
| B、在0.lmol/L Na2SO3的溶液中加入少量NaOH固体,c(Na+)增大,c(SO32-)减小 |
| C、0.lmoI.L-lNH4Cl溶液与0.05moI.L-l NaOH溶液等体积混合溶液中离子浓度:c (Cl-)>c (NH4+)>c (Na+)>c (OH-) |
| D、a mol/L HCN溶液与6 mol/L NaOH溶液等体积混合,所得溶液中c (Na+)>c (CN-),则a一定小于6 |
下列说法正确的是( )
| A、原电池反应是自发的氧化还原反应,盐桥的作用是平衡正负极电荷,形成闭合回路 |
| B、为防止轮船发生腐蚀,往往在轮船外壳焊上金属锌,这是牺牲阴极的阳极保护法 |
| C、精炼铜时,粗铜做阳极,纯铜做阴极,CuSO4是电解质溶液,电解前后溶液浓度不变 |
| D、电镀是特殊的电解,电解前后阴极减少的质量与阳极增加的质量相等 |
 某校研究性学习小组就氮及其化合物展开研究.
某校研究性学习小组就氮及其化合物展开研究.