题目内容
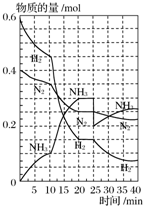 500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3的物质的量变化如图所示,下列说法中正确的是( )
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3的物质的量变化如图所示,下列说法中正确的是( )| A、从反应开始到第一次平衡时,N2的平均反应速率为0.005 mol?L-1?min-1 |
| B、平衡在10 min至20 min的变化,可能是因为增大了容器体积 |
| C、25 min时,分离出了0.1 mol NH3 |
| D、在25 min后平衡向正反应方向移动,新平衡中NH3的体积分数比原平衡的小 |
考点:化学平衡建立的过程,化学平衡的影响因素
专题:化学平衡专题
分析:A.第一次平衡时,时间为20min,氮气的物质的量由0.4mol变为0.25mol,容器容积为2L,根据速率公式可计算出氮气的速率;
B.根据图象知,平衡向正反应方向移动,10min时是连续的,三种气体物质的速率增加倍数相同,说明为使用催化剂;
C.25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3;
D.第25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3,压强减小,据此分析.
B.根据图象知,平衡向正反应方向移动,10min时是连续的,三种气体物质的速率增加倍数相同,说明为使用催化剂;
C.25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3;
D.第25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3,压强减小,据此分析.
解答:
解:A.第一次平衡时,时间为20min,氮气的物质的量由0.4mol变为0.25mol,容器容积为2L,v(N2)=
=0.00625mol/(L?min),故A错误;
B.由图象可知各组分物质的量变化增加,且10min时变化是连续的,20min达平衡时,△n(N2)=0.4-0.25=0.15mol,△n(H2)=0.6mol-0.15mol=0.45mol,△n(NH3)=0.3mol,物质的量变化之比等于化学计量数之比,三种气体物质的速率增加倍数相同,说明10min可能改变的条件是使用催化剂,故B错误;
C.25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3,故C正确;
D.第25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3,由于反应条件为恒容,与原平衡相比,容器内压强减小,则反应进行的程度减小,但达到新平衡后NH3的体积分数比原平衡大,故D错误;
故选C.
| 0.25mol |
| 2L×20min |
B.由图象可知各组分物质的量变化增加,且10min时变化是连续的,20min达平衡时,△n(N2)=0.4-0.25=0.15mol,△n(H2)=0.6mol-0.15mol=0.45mol,△n(NH3)=0.3mol,物质的量变化之比等于化学计量数之比,三种气体物质的速率增加倍数相同,说明10min可能改变的条件是使用催化剂,故B错误;
C.25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3,故C正确;
D.第25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3,由于反应条件为恒容,与原平衡相比,容器内压强减小,则反应进行的程度减小,但达到新平衡后NH3的体积分数比原平衡大,故D错误;
故选C.
点评:本题考查化学平衡的计算、平衡移动以及平衡状态的判断,题目难度中等,注意对图象的分析.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
加水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是( )
A、
| ||
B、
| ||
| C、c(H+)?c(OH-) | ||
| D、n(OH-) |
下列各装置中都盛有0.1mol?L-1 的NaCl溶液,放置相同时间后,锌片的腐蚀速率由快到慢的顺序是( )
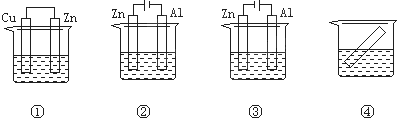

| A、③①④② | B、①②④③ |
| C、②①④③ | D、②①③④ |
改变下列某一条件:①浓度 ②压强 ③温度 ④催化剂,其中一定能使化学平衡发生移动的是( )
| A、①④ | B、②③ | C、①③ | D、②④ |
把铝条放入盛有过量稀盐酸的试管中,不影响氢气产生速率的因素是( )
| A、盐酸的浓度 |
| B、铝条的表面积 |
| C、溶液的温度 |
| D、加少量Na2SO4 |
下列过程或事实不涉及氧化还原反应的是( )
①蔗糖炭化
②用氢氟酸雕刻玻璃
③铁遇冷的浓硫酸钝化
④装碱液的试剂瓶不用玻璃塞
⑤雷雨发庄稼
⑥浓硝酸常显黄色.
①蔗糖炭化
②用氢氟酸雕刻玻璃
③铁遇冷的浓硫酸钝化
④装碱液的试剂瓶不用玻璃塞
⑤雷雨发庄稼
⑥浓硝酸常显黄色.
| A、①③⑤⑥ | B、②④ |
| C、②④⑥ | D、①②③④⑤⑥ |
X、Y、Z三种元素的原子,其最外层电子排布为ns1,3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是( )
| A、X2YZ3 |
| B、X2YZ2 |
| C、X3YZ3 |
| D、XYZ3 |
下列说法正确的是( )
| A、1mol氧气中含有1.204×1024个氧原子,通常情况下占有体积约为22.4L |
| B、1mol臭氧和1.5mol氧气含有相同的氧原子数 |
| C、等体积、浓度均为1mol/L的磷酸和盐酸,电离出的氢离子数之比为3:1 |
| D、欲配制1.00L1.00mol.L-1的NaCl溶液,可将58.5gNaCl溶于1.00L水中 |

