题目内容
IBr的化学性质与卤素单质相似,能与金属反应生成金属卤化物,也可以与水发生如下反应:IBr+H2O=HIO+HBr 下列说法正确的是( )
| A、在IBr中,碘和溴的化合价均为零 |
| B、IBr与水反应时,IBr既是氧化剂又是还原剂 |
| C、IBr与钾反应,化学方程式是2K+IBr=KI+KBr |
| D、IBr与Ca(OH)2溶液反应,产物有CaI2、Ca(BrO)2和H2O |
考点:氯、溴、碘及其化合物的综合应用
专题:
分析:A.I、Br的电负性不同,其吸引电子能力不同;
B.IBr与水反应时,I、Br元素化合价不变;
C.IBr和K反应生成钾盐;
D.IBr和水反应生成的酸再和Ca(OH)2溶液反应生成相应的钙盐.
B.IBr与水反应时,I、Br元素化合价不变;
C.IBr和K反应生成钾盐;
D.IBr和水反应生成的酸再和Ca(OH)2溶液反应生成相应的钙盐.
解答:
解:A.I、Br的电负性不同,其吸引电子能力不同,所以在IBr中I显正化合价、Br显负化合价,故A错误;
B.IBr与水反应时,I、Br元素化合价不变,所以该反应不是氧化还原反应,则IBr既不是氧化剂又不是还原剂,故B错误;
C.IBr和K反应生成钾盐,I、Br的电负性都大于K,所以钾盐中I、Br都体现负化合价,其化学方程式为2K+IBr=KI+KBr,故C正确;
D.IBr和水反应生成的酸再和Ca(OH)2溶液反应生成相应的钙盐,反应方程式为2IBr+2Ca(OH)2=CaBr2+Ca(BrO)2+2H2O,所以产物有CaBr2、Ca(IO)2和H2O,故D错误;
故选C.
B.IBr与水反应时,I、Br元素化合价不变,所以该反应不是氧化还原反应,则IBr既不是氧化剂又不是还原剂,故B错误;
C.IBr和K反应生成钾盐,I、Br的电负性都大于K,所以钾盐中I、Br都体现负化合价,其化学方程式为2K+IBr=KI+KBr,故C正确;
D.IBr和水反应生成的酸再和Ca(OH)2溶液反应生成相应的钙盐,反应方程式为2IBr+2Ca(OH)2=CaBr2+Ca(BrO)2+2H2O,所以产物有CaBr2、Ca(IO)2和H2O,故D错误;
故选C.
点评:本题考查类卤素的性质,侧重考查学生获取信息、利用信息解答问题能力,根据卤族元素单质采用知识迁移方法解答即可,易错选项是B,题目难度不大.

练习册系列答案
相关题目
空气吹出法工艺,是目前“海水提溴”的最主要方法之一.其工艺流程如下,其中不正确的是( )


| A、溴在周期表中位于第四周期VIIA族 |
| B、步骤①中用硫酸酸化可抑制Cl2、Br2与水反应 |
| C、步骤④的离子方程式Br2+SO2+H2O=2H++2Br-+SO42- |
| D、步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物可用分液漏斗分离 |
除去某物质里混有的少量杂质,下列做法中不正确的是(括号内的物质为杂质)( )
| A、KNO3溶液(AgNO3):加足量KCl溶液后过滤. |
| B、NaCl溶液(Na2CO3):加足量盐酸后加热. |
| C、KNO3固体(NaCl):溶解后加热蒸发得浓溶液,降温结晶后过滤. |
| D、NaCl溶液(BaCl2):加过量Na2CO3溶液,过滤,再加适量盐酸并加热. |
下列说法不正确的是( )
| A、△H<0、△S>0的反应在任何温度下都能自发进行 |
| B、NH4HCO3(s)═NH3 (g)+H2O(g)+CO2(g)△H=+185.57 kJ?mol-1能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
| C、因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 |
| D、在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的速率 |
浓度均为0.1mol/L的NaOH溶液与氨水相比较,下列结论正确的是( )
| A、中和HCl的物质的量相同 |
| B、两溶液中所含的OH-数目相同 |
| C、NaOH溶液中c(H+)小 |
| D、氨水中c(OH-)大 |
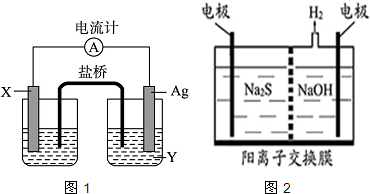
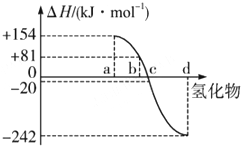 热力学标准态(298K、101kPa)下,由稳定单质发生反应生成1mol化合物的反应热叫该化合物的生成热(△H),图为氧族元素氢化物a、b、c、d的生成热数据示意图,(氧族元素包括氧、硫、硒、碲).试完成下列问题:
热力学标准态(298K、101kPa)下,由稳定单质发生反应生成1mol化合物的反应热叫该化合物的生成热(△H),图为氧族元素氢化物a、b、c、d的生成热数据示意图,(氧族元素包括氧、硫、硒、碲).试完成下列问题: