题目内容
除去某物质里混有的少量杂质,下列做法中不正确的是(括号内的物质为杂质)( )
| A、KNO3溶液(AgNO3):加足量KCl溶液后过滤. |
| B、NaCl溶液(Na2CO3):加足量盐酸后加热. |
| C、KNO3固体(NaCl):溶解后加热蒸发得浓溶液,降温结晶后过滤. |
| D、NaCl溶液(BaCl2):加过量Na2CO3溶液,过滤,再加适量盐酸并加热. |
考点:物质的分离、提纯的基本方法选择与应用,物质的分离、提纯和除杂
专题:
分析:A.硝酸银与KCl反应生成沉淀和硝酸钾,但KCl足量会引入新杂质;
B.碳酸钠与盐酸反应生成氯化钠;
C.二者的溶解度受温度影响不同;
D.氯化钡与碳酸钠反应生成氯化钠,碳酸钠与盐酸反应生成氯化钠.
B.碳酸钠与盐酸反应生成氯化钠;
C.二者的溶解度受温度影响不同;
D.氯化钡与碳酸钠反应生成氯化钠,碳酸钠与盐酸反应生成氯化钠.
解答:
解:A.硝酸银与KCl反应生成沉淀和硝酸钾,但KCl足量会引入新杂质,应加适量的KCl溶液过滤,故A错误;
B.碳酸钠与盐酸反应生成氯化钠,则加足量盐酸后加热可除杂,故B正确;
C.二者的溶解度受温度影响不同,则溶解后加热蒸发得浓溶液,降温结晶后过滤可分离,故C正确;
D.氯化钡与碳酸钠反应生成氯化钠,碳酸钠与盐酸反应生成氯化钠,则加过量Na2CO3溶液,过滤,再加适量盐酸并加热得到NaCl溶液,故D正确;
故选A.
B.碳酸钠与盐酸反应生成氯化钠,则加足量盐酸后加热可除杂,故B正确;
C.二者的溶解度受温度影响不同,则溶解后加热蒸发得浓溶液,降温结晶后过滤可分离,故C正确;
D.氯化钡与碳酸钠反应生成氯化钠,碳酸钠与盐酸反应生成氯化钠,则加过量Na2CO3溶液,过滤,再加适量盐酸并加热得到NaCl溶液,故D正确;
故选A.
点评:本题考查混合物分离提纯等,为高频考点,把握物质的性质及发生的反应等为解答的关键,侧重性质及应用、实验能力的考查,注意除杂的原则,题目难度不大.

练习册系列答案
相关题目
实验室制备氨气,检验是否收集满的正确方法是( )
| A、用手扇动收集的气体,有气味则已收集满 |
| B、将润湿的淀粉KI试纸接近瓶口,试纸变蓝则已收集满 |
| C、将润湿的红色石蕊试纸伸入瓶内,试纸变蓝则已收集满 |
| D、用玻璃棒一端蘸取浓盐酸,接近瓶口,产生大量白烟,证明已收集满 |
下列各物质的分类、名称(或俗名)、化学式都正确的是( )
| A、酸性氧化物 二氧化碳 CO2 |
| B、酸 硫酸 H2S |
| C、碱性氧化物 氢氧化钙 Ca(OH)2 |
| D、碱 纯碱 NaOH |
下列实验操作及其先后顺序均正确的是( )
| A、先装好药品,再检查装置的气密性 |
| B、先用双手捂紧试管,再将导管插入水中检查装置的气密性 |
| C、氢气还原氧化铜的实验,先通一段时间的氢气,后检验氢气纯度,再加热 |
| D、稀释浓硫酸时,先在烧杯里倒入浓硫酸,再小心倒入水并不断搅拌 |
IBr的化学性质与卤素单质相似,能与金属反应生成金属卤化物,也可以与水发生如下反应:IBr+H2O=HIO+HBr 下列说法正确的是( )
| A、在IBr中,碘和溴的化合价均为零 |
| B、IBr与水反应时,IBr既是氧化剂又是还原剂 |
| C、IBr与钾反应,化学方程式是2K+IBr=KI+KBr |
| D、IBr与Ca(OH)2溶液反应,产物有CaI2、Ca(BrO)2和H2O |
化肥和农药对农牧业的增产增收起重要作用,但使用不当也会给人类和环境带来危害.下列关化肥或农药的使用描述不正确的是( )
| A、(NH4)2SO4的大量使用可能造成土壤的碱化 |
| B、磷肥的大量使用可能造成水体富营养化 |
| C、农药的使用可能影响害虫与其天敌之间的生态平衡 |
| D、家蚕吞食喷洒过农药的桑叶,可能引起中毒 |


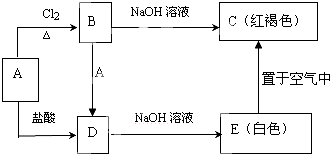 某金属A及其化合物之间有如下转化关系.
某金属A及其化合物之间有如下转化关系.