题目内容
下列离子方程式正确的是( )
| A、NaHSO4与过量的Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B、碳酸氢铵溶液中加入过量氢氧化钠溶液 HCO3-+OH-=CO32-+H2O |
| C、碳酸镁溶于硝酸中:CO32-+2H+=H2O+CO2↑ |
| D、硫化钠溶于水中:S2-+2H2O=H2S↑+2OH- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.二者反应生成硫酸钡、氢氧化钠和水;
B.二者反应生成碳酸钠、一水合氨和水;
C.难溶物写化学式;
D.硫离子水解生成硫氢根离子和氢氧根离子.
B.二者反应生成碳酸钠、一水合氨和水;
C.难溶物写化学式;
D.硫离子水解生成硫氢根离子和氢氧根离子.
解答:
解:A.二者反应生成硫酸钡、氢氧化钠和水,离子方程式为Ba2++OH-+H++SO42-=BaSO4↓+H2O,故A正确;
B.二者反应生成碳酸钠、一水合氨和水,离子方程式为NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O,故B错误;
C.难溶物写化学式,离子方程式为MgCO3+2H+=Mg2++H2O+CO2↑,故C错误;
D.硫离子水解生成硫氢根离子和氢氧根离子,离子方程式为S2-+H2O?HS-+OH-,故D错误;
故选A.
B.二者反应生成碳酸钠、一水合氨和水,离子方程式为NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O,故B错误;
C.难溶物写化学式,离子方程式为MgCO3+2H+=Mg2++H2O+CO2↑,故C错误;
D.硫离子水解生成硫氢根离子和氢氧根离子,离子方程式为S2-+H2O?HS-+OH-,故D错误;
故选A.
点评:本题考查了离子方程式正误判断,明确物质的性质及离子方程式书写规则即可解答,注意AB中反应物的量,反应物的量不同其产物不同,注意D中硫离子水解程度较小,以第一步水解为主.

练习册系列答案
相关题目
下列说法正确的是( )
| A、含有金属阳离子的晶体一定是离子晶体 |
| B、固态和熔融状态可导电,投入水中形成的水溶液也可导电,该物质可能是金属晶体 |
| C、白磷晶体中只存在一种作用力,即分子间作用力 |
D、如图,NaCl晶体中,距离最近的Na+组成的最小多面体是正八面体 |
物质的量浓度相同的下列溶液,pH由大到小排列正确的是( )
| A、Ba(OH)2、Na2SO3、FeCl3、KCl |
| B、Na2CO3、NaHCO3、KNO3、NH4Cl |
| C、NH3?H2O、H3PO4、Na2SO4、H2SO4 |
| D、HCl、CH3COOH、C2H5OH、Na2SiO3 |
下列说法正确的是( )
| A、丙烷是直链烃,所以分子中3个碳原子也在一条直线上 |
| B、丙烯所有原子均在同一平面上 |
C、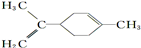 所有碳原子一定在同一平面上 所有碳原子一定在同一平面上 |
D、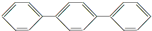 至少有16个原子共平面 至少有16个原子共平面 |
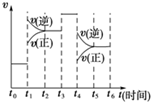 反应N2(g)+3H2(g)
反应N2(g)+3H2(g)
| ||
| △ |
| A、t0~t1 |
| B、t2~t3 |
| C、t3~t4 |
| D、t5~t6 |
氯化溴(BrCl)和Br2、Cl2具有相似的性质,下列有关氯化溴性质的判断中错误的是( )
| A、在CCl4中的溶解性BrCl<Br2 |
| B、BrCl氧化性比Br2强,比Cl2弱 |
| C、沸点BrCl>Br2 |
| D、常温下BrCl可与NaOH溶液反应生成NaCl和NaBrO |
用NA表示阿伏加德罗常数的值,下列叙述错误的是( )
| A、含有NA个氢原子的氢气在标准状况下的体积约为11.2L |
| B、25℃,1.01×105Pa,64g SO2中含有的原子数为3NA |
| C、在常温常压下,35.5g Cl2含有的分子数为0.5NA |
| D、标准状况下,11.2L H2O含有的分子数为0.5NA |