题目内容
 反应N2(g)+3H2(g)
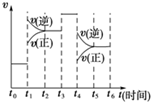
反应N2(g)+3H2(g)
| ||
| △ |
| A、t0~t1 |
| B、t2~t3 |
| C、t3~t4 |
| D、t5~t6 |
考点:化学反应速率变化曲线及其应用
专题:化学反应速率专题
分析:可逆反应N2(g)+3H2(g)?2NH3(g)△H<0,该反应为体积减小的放热反应,改变反应条件平衡移动,根据各时刻的速率变化判断平衡移动移动方向,据此判断NH3的含量变化,据此解答.
解答:
解:可逆反应N2(g)+3H2(g)?2NH3(g)△H<0,该反应为体积减小的放热反应,
t0~t1,正、逆反应速率相等,平衡不移动;
t1~t2,正、逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆反应方向移动,导致氨气的含量降低,氨气含量较t0~t1低;
t2~t3,正、逆反应速率相等,处于平衡状态,氨气的含量不变,氨气含量较t1~t2低;
t3~t4,正、逆反应速率都同等程度的增大平衡不移动,氨气的含量不变,氨气含量与t2~t3相同;
t4~t5,正、逆反应速率都降低,但逆反应速率大于正反应速率,导致平衡向逆反应方向移动,氨气的含量降低;
t5~t6,正、逆反应速率相等,平衡不移动,氨气的含量不变,氨气含量较t4~t5低;
所以平衡混合物中氨的百分含量最低的时间段是t5~t6,NH3的含量最高的一段时间是t0~t1,
故选A.
t0~t1,正、逆反应速率相等,平衡不移动;
t1~t2,正、逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆反应方向移动,导致氨气的含量降低,氨气含量较t0~t1低;
t2~t3,正、逆反应速率相等,处于平衡状态,氨气的含量不变,氨气含量较t1~t2低;
t3~t4,正、逆反应速率都同等程度的增大平衡不移动,氨气的含量不变,氨气含量与t2~t3相同;
t4~t5,正、逆反应速率都降低,但逆反应速率大于正反应速率,导致平衡向逆反应方向移动,氨气的含量降低;
t5~t6,正、逆反应速率相等,平衡不移动,氨气的含量不变,氨气含量较t4~t5低;
所以平衡混合物中氨的百分含量最低的时间段是t5~t6,NH3的含量最高的一段时间是t0~t1,
故选A.
点评:本题考查了化学平衡移动图象等,难度中等,关键是根据图象中反应速率的变化判断平衡移动的方向.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
在集气瓶中使用甲烷与氧气混合,点燃,进行爆炸性试验,下列甲烷与氧气的体积比中爆炸声最大的是( )
| A、1:1 | B、1:2 |
| C、1:3 | D、3:1 |
用下列实验装置进行的实验中,不能达到相应实验目的是( )
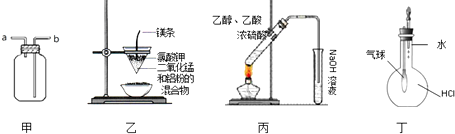

| A、装置甲:气体从a口进入,收集NH3 |
| B、装置乙:可制得金属锰 |
| C、装置丙:实验室制取乙酸乙酯 |
| D、装置丁:验证HCl气体在水中的溶解性 |
物质的量浓度、体积都相同的一元酸和一元碱恰好中和时,溶液将( )
| A、显酸性 | B、显中性 |
| C、显碱性 | D、无法确定酸碱性 |
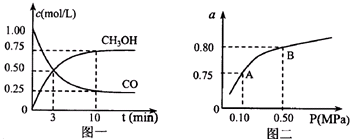
一定温度下,将1mollCO与2molH2和催化剂一起放入容积恒定密闭容器中反应:CO(g)+2H2(g)?CH3OH.测得平衡时生成CH3OH0.65mol.若此时再通入H2 2mol.则重新达到平衡时,CH3OH的物质的量可能是( )
| A、0.65 | B、0.72 |
| C、1.00 | D、1.30 |
下列离子方程式正确的是( )
| A、NaHSO4与过量的Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B、碳酸氢铵溶液中加入过量氢氧化钠溶液 HCO3-+OH-=CO32-+H2O |
| C、碳酸镁溶于硝酸中:CO32-+2H+=H2O+CO2↑ |
| D、硫化钠溶于水中:S2-+2H2O=H2S↑+2OH- |
在一定条件下,C(s)+H2O(g)?CO(g)+H2(g)△H>0在一容积固定的密闭容器中放入足量的焦炭与一定量的水蒸气进行反应,下列有关图象正确的是( )
A、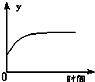 表示反应进行过程中气体平均相对分子质量的变化 |
B、 表示反应进行过程中气体密度的变化 |
C、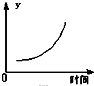 表示反应达到平衡后,移去一些焦炭后水蒸气的百分含量的变化(忽略表面积的影响) |
D、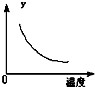 表示反应达到平衡后,升高温度CO的百分含量的变化 |